Есть такое сентиментальное клише: рождение ребёнка – это чудо. Но вы даже не представляете, насколько это на самом деле верно с точки зрения биологии. Посудите сами: из двух взрослых организмов природа создаёт один – или несколько – молодых. Представьте себе: женщине 37, мужчине 45, они встречаются и заводят клеточку, у которой отброшены все признаки старения.
Потом эта клеточка делится-делится-делится – и получается новый организм, состоящий из триллиона клеток. Затем этот организм находит партнёра и – если он или она не чайлдфри, конечно – заводит своё потомство. Каждый из нас – это продукт непрерывной цепочки делящихся клеток. И все мы восходим к нашим одноклеточным предкам, которые обитали на Земле более миллиарда лет назад.Омоложение возможно в процессе размножения. И тут кто-то скажет: ха, всё дело в сексе! Взрослые занялись любовью – взяли свои одноклеточные яйцеклетку и сперматозоид – и случилась магия. Я вас расстрою: секс тут ни при чём. Некоторые организмы воспроизводят себя бесконечным копированием – причём они делают это на протяжении десятков тысяч лет. Например, в Тасмании растёт симпатичный блестящий кустик – королевский остролист (Lomatia tasmanica). В высоту он может достигать 8 м, но интересен кустик не этим. Дело в том, что остролист абсолютно бесплоден – у него нет ни семян, ни плодов. Размножается он черенками – и всё его потомство абсолютно генетически идентично оригиналу. Вообще популяция остролиста – лишь около нескольких сот особей. Но при этом предок всех остролистов “жил” 43 тыс. лет назад. 43 тыс. лет остролист занимается клонированием!
Как размножаются звёзды
А ещё в американском штате Мичиган растёт гриб Armillaria gallica, он же опёнок толстоногий. Учёные выяснили, что все опята толстоногие – это единый организм с одной грибницей. Armillaria gallica около 2500 лет, её масса составляет около 400 т, а ещё своим мицелием гриб покрывает 70 гектаров площади под лесом. А в штате Орегон растёт другой гриб, Armillaria ostoyae, опёнок тёмный. В 1998 году исследователи определили, что грибница этого опёнка – не отдельные скопления, растущие по всему лесу, а гигантский целостный живой организм. Возраст Armillaria ostoyae – около 8500 лет, а занимает он площадь более 880 гектаров. Учёные даже прозвали его “чудовищным грибом”.
Клонировать себя могут не только грибы и растения, но и, например, морские звёзды. Этим иглокожим можно отрезать одну ножку – и из ножки возникнет новое существо. Морские звёзды размножаются как вегетативно – то есть от них отваливается кусочек, из которого вырастает клон взрослой особи – так и половым путём. Да, звёзды тоже занимаются сексом – и на свет появляется генетически отличное потомство, что ускоряет эволюцию.
К чему я клоню? К тому, что в природе омоложение случается не только благодаря сексу. Некоторые земные организмы могут жить ужасно долго, просто воспроизводя свои молодые копии. Люди, которые философствуют, мол, всё умирает, всё тленно, “против роста энтропии не попрёшь”, на самом деле ошибаются.
Как спастись на “Титанике”
Представьте, что мы - “Титаник”, который несётся в сторону айсберга, то есть смерти. На “Титанике” находится множество пассажиров – это наши клетки. Есть клетки привилегированные – это пассажиры первого класса, у которых под рукой шлюпки. Об этих клетках всю жизнь заботились – чтобы они хорошо питались и не болели. Какие это клетки? Конечно же половые, ведь эволюция “заботится” прежде всего о передаче наших генов, в следующие поколения, а без половых клеток это невозможно. А вот 99% остальных клеток шлюпками не обеспечены. Обидно, что им суждено погибнуть, учитывая, что это и есть мы!
Но что если те блага, которые предназначены эволюцией для привилегированного класса клеток, могли бы достаться всему организму? Что, если мы раскроем и позаимствуем механизмы, омолаживающие половые клетки и эмбрионы, и устроим в организме равенство и своеобразный “коммунизм”?
Алексей Оловников и Ахиллесова пята копирования ДНК
Какие преграды могут встретиться на пути к бесконечному самоомоложению? В 1951 году биологи Леонард Хейфлик и Пол Мурхед показали, что существует предел количеству делений у взрослого организма. Учёные помещали клетки в пробирку – и там они делились 40-60 раз, а дальше старели и уже не делились. Так в науку вошёл термин “предел Хейфлика”, который означает границу делений соматических клеток, то есть клеток тела.
Есть мнение, что этот предел – один из механизмов старения. Причём обратите внимание, что клеток, используемых в размножении, он очевидно не касается. Возникает вопрос: а 40-60 делений – это много или мало? Если мы возьмём одну клетку и последовательно поделим её 50 раз (то есть возведём 2 в 50 степень), получится 1 126 триллионов клеток. Столько клеток содержится примерно в тридцати людях – ведь всего у человека в теле порядка 37 триллионов клеток. Из одной клетки можно было бы “сделать” 30 людей – но у человека-то клетки постоянно обновляются, причём обновляются достаточно быстро. Каждый день у человека заменяется 0,25% клеток, то есть четверть процента. Получается, что одна клетка способна обеспечить 30 лет жизни. Если добавить одно деление (получится 51) — это уже 60 лет жизни. Все мы начинаемся с одной-единственной клетки. И если бы эта клетка могла поделиться всего 40 раз, то у нас просто бы не хватило клеток, чтобы получить хотя бы одного человека – мы бы даже не выросли. Поэтому от того, сколько раз могут поделиться наши клетки, зависит наше с вами будущее.
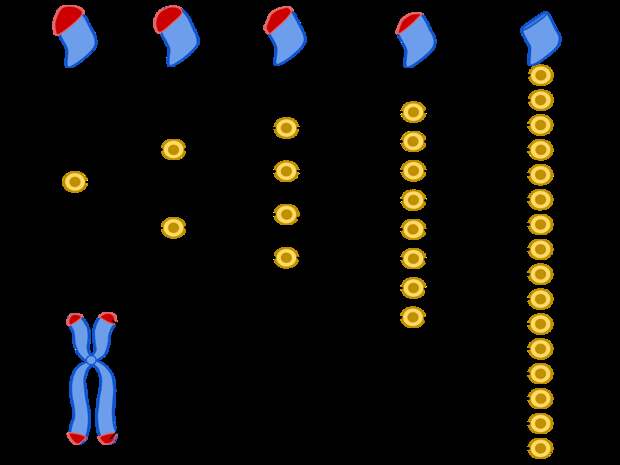
Ещё в 1971 году отечественный учёный Алексей Оловников обратил внимание на ахиллесову пяту копирования ДНК. Как происходит это копирование? Двойная спираль расплетается на две одиночных ниточки – одна половина делает одну копию, а другая вторую. Но этот процесс не может начаться с нуля. Нужен праймер – затравка, которая показывает, откуда начинать копирование. Она делается из РНК, которая потом удаляется. В середине хромосом дырки после удаления РНК заменяются на ДНК, а на концах хромосом этого не происходит. И поэтому каждый раз, когда ДНК копируется, она укорачивается на длину маленького “выпавшего” куска.
С такой проблемой не сталкиваются, например, бактерии. У них молекула ДНК – кольцевая, поэтому копирование можно начать с любого места. А вот у человеческих линейных хромосом есть начало и конец. И получается, что с возрастом при делении клеток эти концы медленно укорачиваются. По мнению Алексея Оловникова, наши с вами концевые участки хромосом что-то в природе должно восстанавливать. Учёный считал, что есть способ избавиться от предела делений – и это должно помочь в борьбе со старением.
Почему теломераза – это важно
Через 11 лет учёные Элизабет Блэкбёрн, Джек Шостак и Кэрол Грейдер подтвердили догадки Алексея Оловникова и открыли механизмы защиты хромосом теломерами и фермент теломеразу. Теломераза умеет достраивать кончики хромосом. Сначала исследователи обнаружили этот фермент у одного вида инфузорий, а затем – у человека. Оказалось, что теломераза – это не никому не доступный священный Грааль. Она есть во всех наших клетках, однако в некоторых клетках этот фермент “спит”. В полную силу теломераза работает в стволовых, зародышевых, половых, эмбриональных и некоторых других клетках. И в них кончики хромосом не укорачиваются.
Сегодня в науке общепринято, что теломераза – это важный и полезный работающий фермент. Хотя раньше были скептики, которые, например, не верили в возможность клонирования. Они считали, что клонирование невозможно, потому что во взрослых организмах клетки уже старые, часть предела Хейфлика в них отыграна, молодую копию создать просто не получится. Однако выяснилось, что при клонировании в молодом эмбрионе активируется теломераза, кончики хромосом достариваются до нормального размера – и на свет появляется юная овечка Долли. Кстати, выяснилось, что теломераза очень хорошо работает у уже упомянутых морских звёзд, когда им нужно заново вырастить свои конечности.
Существуют и обратные ситуации, когда из-за генетической мутации кончики хромосом не могут достроиться – и теломеры очень быстро укорачиваются, что приводит к серьёзным генетическим заболеваниям. Пример такого заболевания – врождённый дискератоз. Пациенты с этим недугом страдают от пятен на коже, у них быстро седеют волосы, часто отсутствуют ногти… Но главные повреждения происходят не на поверхности организма, а внутри. В частности, из-за нарушений работы костного мозга появляется иммунодефицит, в 70 раз увеличивается риск некоторых онкологических заболеваний, в 500 раз повышается риск ряда сердечно-сосудистых заболеваний. Человек “ускоренно” стареет и живёт гораздо меньше, чем другие люди.
В общем, как и предполагал Алексей Оловников, теломеры, теломераза и старение – вещи связанные. Более того, оказалось, что, чем быстрее укорачиваются теломеры у разных видов животных, тем ниже их продолжительность жизни. И тогда же возникла идея борьбы со старением путём активации теломеразы и наращивания теломер. Правда, проблема заключалась в том, что теломераза также активна в раковых клетках, которые должны очень активно делиться. Учёные опасались, что наращивание теломер приведёт к повышенному риску рака. Поэтому исследователи вывели специальных мышей, у которых изначально были продублированы три противораковых гена. А ещё грызунам добавляли дополнительный ген теломеразы. Идея была такая: противораковые механизмы подавят онкологические заболевания – и теломераза будет не так вредна. В ходе исследования учёным удалось продлить жизнь мышам на 9-20% по сравнению с продолжительностью жизни грызунов, которым просто дублировали антираковые гены. А если сравнить совокупный эффект и активации теломеразы, и удвоения противораковых генов, то мы увидим, что продолжительность жизни грызунов увеличится аж на 40%.
Другая команда учёных просто наращивала мышам теломеры. Оказалось, что потомки грызунов с длинными теломерами живут дольше своих “обычных” сородичей – примерно на 10%. А ещё, вопреки теоретическим представлениям, такие мыши болеют раком не чаще, а реже.
Вакцина “Спутник” и факторы Яманаки
К сожалению, людям такой “мышиный” способ борьбы со старением не подходит. Ведь мыши в экспериментах уже рождались с усиленной теломеразой. А с чем родились, с тем и живём. Зато человеку может помочь генная терапия. Для тех же мышей её уже провели. Дело обстояло так: учёные положили внутрь оболочки вируса фрагмент ДНК с геном теломеразы, ввели его взрослым мышам. Это привело к продлению жизни примерно на 10-20%. И, что важно, случаи рака среди ГМ-грызунов не участились.
В 2022 году исследователи сделали похожую терапию, но на этот раз использовали “заразный” вирусный вектор, который умеет себя воспроизводить. Тоже с геном теломеразы. С этим вирусом мышам продлили жизнь больше, чем на 40%. В общем, у нас две хороших новости. Первая: изучая чудо омоложения, учёные обнаружили, что есть фактор старения, который можно “откатывать” назад. Вторая: это можно сделать очень дёшево. Недавно мы столкнулись с пандемией коронавируса, вакцины против которого стали доступны легко и быстро. При этом многие вакцины от ковида представляли собой сложные биотехнологические продукты: в вирусную оболочку препарата “засунули” ген коронавируса. Тут история похожая: ген теломеразы нужно “засунуть” в вирусную оболочку. Я думаю, такой укол может стоить столько же, сколько прививка “Спутник”.
Второй секрет бессмертия: откат до “заводских настроек” генома
Но есть и плохие новости. Недостаточно удлинить теломеры, чтобы победить старение. Потому что укорачивание теломер – лишь один из факторов старения. Расскажу подробнее: у нас есть много типов клеток. Генетически клетки вроде бы идентичны, но при этом в них работают разные гены. Потому что к генам могут “приделываться” разные белки и химические метки. Эти эпигенетические метки, в свою очередь, активируют или выключают те или иные гены. Это нормально и очень нужно: каждый тип клеток выполняет свою работу – одни гены в нём работают, а другие “спят”.
Как всё это дело мешает бессмертию? Когда мы стареем, эпигенетические метки могут стираться или образовываться в ненужном месте. В одних клетках перестают работать гены, которые должны в них работать, в других – включаются гены, которые должны спать. Возникает “эпигенетическое старение”, которое настолько ярко выражено, что исследователи научились по нему определять биологический возраст человека и даже в некоторой степени предсказывать, сколько ему осталось жить.
К счастью, эти эпигенетические метки можно сбросить до заводских настроек. Это и происходит в эмбрионе, причём в несколько волн. И мы умеем этот процесс воспроизводить – причём в любом типе клеток. За это надо сказать спасибо Синьи Яманаке: учёный смог отредактировать 4 гена – те самые “факторы Яманаки” – ввести их во взрослую клетку и получить “откат” этой клетки к эмбриональному состоянию. Далее обновлённую клетку можно превратить в разные типы клеток – в мышечную, нервную или любую другую. Так мы можем омолаживать организм. Кстати, по поводу факторов Яманаки высказывались опасения – мол, тоже рак проявится. Действительно, один из факторов Яманаки оказался онкогеном – но выяснилось, что, если его выкинуть, то оставшихся трёх генов будет достаточно для “омолаживания”.
Так давайте омолаживать все клетки в стареющих организмах! Увы, ни к чему хорошему это не приведёт: организм просто превратится в омоложенную бесформенную клеточную массу. Нам нужны специализированные клетки, поэтому надо как-то ограничить действие факторов Яманаки. Поэтому учёные решили, что стоит включать факторы Яманаки циклически – например, сделать так, чтобы эти гены работали только в присутствии некоторого вещества, которое поступает в организм раз в 1-2 недели. Таким вот способом учёным уже удалось частично “омолодить” мышей. Пока что не очень сильно, но направление очень перспективно. Недавно основатель Amazon Джеф Безос вложился в компанию Altos Labs, которая намерена заниматься эпигенетическим омоложением в медицинских целях.
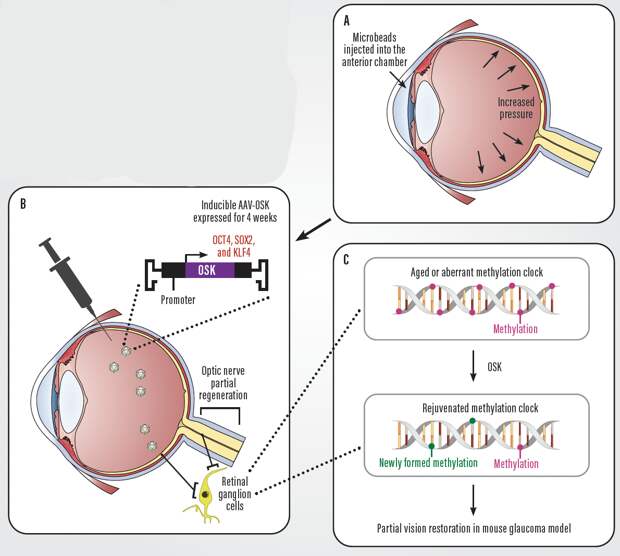
Одна из самых впечатляющих работ по применению эпигенетического отката была сделана на грызунах. Мышам с глаукомой ввели факторы Яманаки и восстановили им зрение. Возможно, в будущем подобные опыты станут проще и доступней: недавно исследователи и вовсе перешли к использованию малых молекул, которые подобраны так, чтобы имитировать действие факторов Яманаки.
Третий секрет бессмертия: избавляемся от мусора
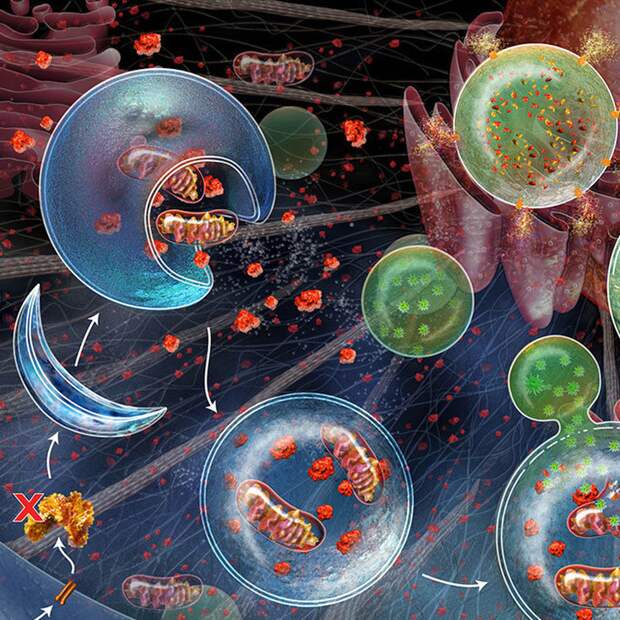
В наших клетках накапливается мусор разной формы – повреждённые митохондрии, неправильно свёрнутые белки… Как нам от него избавиться?. Помочь может аутофагия - способность клеток переваривать свои ненужные, вредные или поломанные компоненты. Это делается с помощью аутофагосом – сферических структур с двухслойными мембранами. Аутофагосомы работают так: один мембранный пузырёк захватывает кусок мусора. Второй содержит ферменты, которые могут растворять мусор (как бы чистящие средства). Два пузырька слипаются – и начинается переваривание. При этом второй пузырёк, лизосому, нужно активировать: накачать в него протоны, закислить среду внутри – тогда он будет готов растворять мусор. Как показали опыты на круглых червях, если встречаются сперматозоид и яйцеклетка, весь процесс начинает работать на полную мощность: вторые пузырьки накачиваются кислотой, а первые активно нападают на мусор.
На такой клининг активно тратится энергетический “бензин” клетки, АТФ. Постоянно с такой силой убираться клетка не может. Зато в развивающемся эмбрионе начинается генеральная уборка, которая очищает его от всего мусора, накопившегося за жизнь. Слияние сперматозоида и яйцеклетки – очень важный момент. Вся жизнь потомка зависит от единственной клетки. Поэтому её нужно привести в идеальный вид – так же, как мы вызываем дорогой клининг в квартиру перед заселением жильца.
Ещё в нашем организме есть “роботы-пылесосы”. Это протеасома – огромный комплекс, который плавает внутри клетки и нарезает белки на куски. Он похож на шредер, который перерабатывает ненужные белки. Исследования показывают, что в эмбриональных клетках, а также в клетках, искусственно омоложенных факторами Яманаки, эти протеасомы выходят на максимальную мощность и “рубят” максимум мусорных белков.
Чем опасны поломанные митохондрии
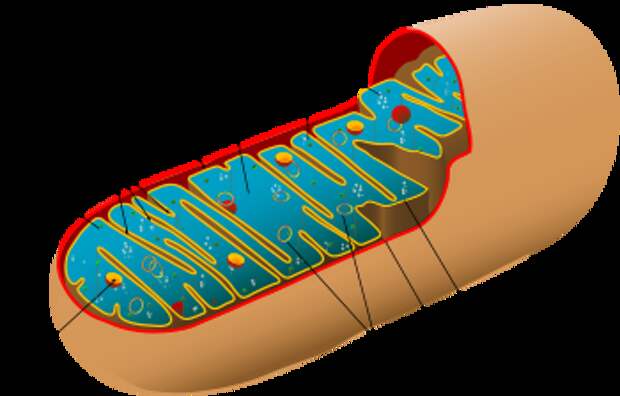
Обычный белковый мусор в нашем организме бывает не так страшен, как плохо работающие митохондрии, наши дыхательные органеллы, у которых есть своя ДНК. Когда клетка делится, она наследует лишь часть мусора, который там плавает, то есть каждый потомок становится “чище”. Но митохондрии, в том числе повреждённые, умеют делиться. То есть на выходе мы получаем сломанный механизм, который размножается.
Сохранить качество митохондрий особенно важно при размножении. Передаются они преимущественно по материнской линии, от матери ребенку. Митохондриальные заболевания могут приводить к серьезным последствиям. К счастью, такое встречается редко – потому что механизм избавления от плохих митохондрий очень эффективен. Учёные провели опыты на мышах – ломали им митохондрии. Выяснилось, что уже через несколько поколений поломки исчезали!
Как работает процесс очистки от плохих митохондрий? Дело в том, что женское тело штампует огромное количество предшественников яйцеклеток – гораздо больше, чем ему когда-либо понадобится. Но большинство из них не станет настоящими яйцеклетками: они погибнут из-за программируемой смерти. Причём эту смерть запускают именно плохие митохондрии. В результате в полноценную яйцеклетку вырастет, скорее всего, самая здоровая клетка-предшественница. А плохие яйцеклетки с поломанными митохондриями так и не разовьются в готовую для оплодотворению клетку.
К сожалению, из этой клеточной “евгеники” мы мало что можем взять, потому что не знаем, как устроить отбор хороших митохондрий в неполовых клетках. Но зато есть другой процесс, который избавляет наши взрослые клетки от плохих митохондрий – митофагия, причём устроен он очень интересным образом.
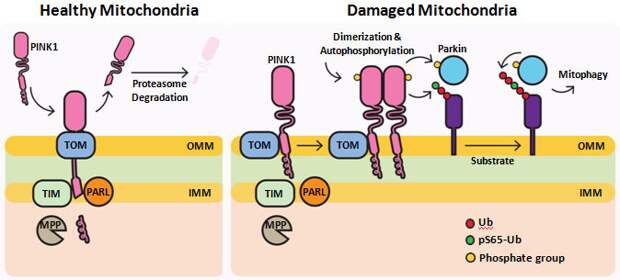
- Задача митохондрий – дышать. При этом внутри у них возникает отрицательный электрический потенциал, а снаружи положительный. Но если митохондрия работает плохо, этой разницы потенциалов нет;
- Есть такой белок – PINK1. В норме он прилипает к митохондриями, но ненадолго. “Заряженная митохондрия” его процессирует и “отпускает”. Но если это не происходит, то PINK1 накапливается на поверхности;
- К PINK1 прилипает белок под названием “PARKIN”;
- Если на митохондрию прилип “PARKIN”, клетка знает, что митохондрия плохая, надо её переварить;
- Если PINK1 или белок PARKIN затронула мутация, это может привести к раннему развитию болезни Паркинсона – из-за того, что PARKIN работает плохо, а в клетках копятся плохие митохондрии. Если мы найдём лекарство против Паркинсона, то, возможно, сможем давать его и здоровым людям – чтобы улучшать у них чистку плохих митохондрий и продлевать им жизнь. Да, болезнь Паркинсона, отчасти связана с нарушением работы митохондрий в нейронах нашего головного мозга.
Я перечислил разные процедуры по уборке, починке и обновлению клетки, чтобы реализовать “чудо бессмертия”. Предположим, теломеры мы нарастили, эпигенетические маркеры сбросили, клеточный мусор убрали, митохондрии прочистили… Но нам предстоит ещё одна миссия – победить мутации. Если мутация уже возникла, при делении клеток она будет себя воспроизводить. Именно из-за этих ошибок ДНК может возникать рак и другие неприятные вещи. Починка ДНК существует – и она, конечно же, лучше всего работает в половых клетках.
Есть такой ген – АTM, который фиксирует повреждения в ДНК и сообщает об этом. В результате активируются ферменты, которые чинят ДНК. Или клетку с мутацией просто уничтожают! Опыты на круглых червях показали, что АТМ работают более активно в клетках гермальной линии, то есть в половых клетках и предшественниках. Потому что червяк живёт примерно недели две, если у него вдруг появится мутация, которая может привести к раку, это не так страшно – всё равно смерть скоро наступит. А вот клетки гермальной линии очень важны – ведь червям не нужно нежизнеспособное потомство, которое не передаст свои гены дальше.
Мы не червяки. И у нас АТМ активно работает не только в клетках гермальной линии. Но с возрастом активность АТМ у нас снижается. А ещё у людей есть генетическая болезнь, при которой этот белок отключается вовсе – синдром Луиса-Барра.
Не знаю, хранит ли АТМ в себе секрет омоложения. Но это история о том, что механизмы починки ДНК в разных типах клеток работают по-разному. И мы теоретически можем разработать такую генную инженерию, которая поможет чинить нашу ДНК в обычных клетках так же эффективно, как и в половых. Тогда наши органы будут сохраняться гораздо дольше.
Долой привилегии пассажиров первого класса! Молодость рабочим клеткам организма!
Список литературы: https://docs.google.com/document/d/1BVxzaV_iXEQvEG5CpHIIs5tdmArdCCPfdZEc60LHWA0/edit

Свежие комментарии