
Захаров Сергей Геннадьевич, к.м.н., заместитель председателя совета молодых ученых и специалистов МОНИКИ; Старший научный сотрудник отделения; врач-гематолог ЦОЗ МО; доцент кафедры клинической трансфузиологии и гематологии
[embedded content]
Практически любое заболевание человека неизбежно отражается на тех или иных показателях анализа крови, и для правильной их интерпретации врачу, вне зависимости от его специальности, необходимо понимать, что есть норма и патология.
Одним из наиболее клинически важных синдромов, выявляющихся по анализам крови, является анемия. Причинами анемии могут стать различные заболевания, сопровождающиеся снижением числа эритроцитов или уровня гемоглобина в крови из-за кровопотери, нарушения продукции, повышенного разрушения или их сочетания [1, 2]. Об алгоритме диагностики анемии, ее клинических проявлениях, профилактике, выявлении и лечении наиболее распространенного вида анемии – железодефицита, рассказал в своей лекции «Тревожные знаки в анализе крови: как избежать катастрофы» Захаров Сергей Геннадьевич, к.м.н., врач-гематолог центра орфанных заболеваний МО, старший научный сотрудник отделения клинической гематологии и иммунотерапии и доцент кафедры гематологии и клинической трансфузиологии МОНИКИ им М.Ф. Владимирского, эксперт качества медицинской помощи в РФ и эксперт Российского научного фонда.Анемия может представлять собой как первичное (гематологическое) заболевание, так и вторичный, по отношению к другим соматическим нарушениям, синдром. Установить корень проблемы и верно диагностировать проблему поможет, во-первых, тщательный сбор анамнеза. Сергей Геннадьевич подчеркнул, что чем больше специалист разговаривает с пациентом, тем больше информации может получить. Нередко, когда возникает необходимость установить наличие корреляции между временем возникновения каких-либо симптомов и изменениями показателей крови, только сам пациент, а не его амбулаторная карта, может прояснить ситуацию. Направить диагностический поиск в нужное русло и выявить причину анемии поможет также информация о перенесенных заболеваниях, особенностях питания, производственных вредностях, приеме тех или иных лекарственных препаратов. Так, например, наличие в анамнезе пациента сахарного диабета может заставить заподозрить поражение почек, и анемия в данном случае будет следствием хронической почечной недостаточности и нарушения продукции эритропоэтина. У пациента с гипотиреозом в анамнезе причиной анемии может служить снижение реактивности эритропоэза на гипоксию и нарушение чувствительности эритроидных клеток. В данном случае пациента необходимо направить к эндокринологу для лечения первичного заболевания.
Жалобы у пациентов с анемией, как правило, носят неспецифический характер, и включают слабость, повышенную утомляемость, раздражительность, сонливость, головокружение, шум в ушах, мелькание «мушек перед глазами», сердцебиение в покое или при минимальной физической нагрузке, появление одышки [1-4]. Эти признаки могут быть проявлением самых разных заболеваний, однако наличие ключевого симптома – нарастающей слабости, является поводом для тщательного обследования пациента на анемию, которое всегда должно начинаться с назначения анализа крови. В более редких случаях анемия сопровождается специфическими симптомами и группой симптомов, которые позволят, при грамотном сборе анамнеза и объективном осмотре, быстро заподозрить правильный диагноз:
- желтуха (в таких случаях диагноз гемолитической анемии можно поставить практически «в дверях» и незамедлительно направить пациента на анализ крови)
- парестезия, сглаженность сосочков языка и его болезненность (свидетельствуют в пользу В12-дефицитной анемии)
- патоосмия и патофагия (извращение вкуса и запахов), койлонихия («ложечные ногти») (симптомы требуют клинической настороженности в отношении железодефицитной анемии)

Важно помнить, что диагноз анемии устанавливается только после проведения обследования больного. И только диагноз, основанный на лабораторных данных, дает право начать соответствующее лечение [1]. Подозрение, сформировавшееся у врача во время первичного приема, даже при наличии у пациента специфических симптомов, не может являться основанием для начала терапии, поскольку неправильное лечение может, как минимум, смазать лабораторную картину и препятствовать установлению верного диагноза, и, как максимум, привести к более серьезным последствиям.
Диагностика анемии требует минимума обязательных исследований [1-4]:
1) общий анализ крови с морфологическим анализом мазка крови и оценкой лейкоцитарной формулы.
Спикер подчеркнул роль врача-лаборанта в диагностике анемий и других гематологических заболеваний. По его словам, на данном этапе развития медицины ни один суперсовременный автоматический счетчик крови не может заменить исследование мазка периферической крови глазом человека, которое является наиболее информативным и полезным методом диагностики. Исследование мазка крови также позволит оценить эритроидный, тромбоцитарный и гранулоцитарный ростки. При оценке результатов анализа важно помнить о том, что нормальная гомеостатическая реакция организма на анемию – активация эритропоэза, и если система обратной связи функционирует нормально, то степень активации эритроидного ростка гемопоэза прямо пропорциональна степени тяжести анемии. Поэтому, если результаты анализа крови свидетельствуют о ретикулоцитозе, следует задуматься о его причине, выявить которую необходимо с помощью дополнительных методов обследования.
Визуальное исследование мазка крови крайне информативно для определения гематологической природы анемии. Характерная форма эритроцитов (сфероциты, акантоциты, шизоциты, пойкилоциты, мишеневидные, серповидные и др.) часто является ключевым критерием диагностики той или иной гематологической проблемы.
При подозрении на гематологическое заболевание пациент направляется к гематологу, который назначает миелограмму (морфология жидкой части костного мозга), трепанобиопсию (гистологическое исследование костного мозга), или специфические лабораторные методы (прямая и непрямая проба Кумбса, электрофорез гемоглобина, определение ферментов эритроцита и т.д) [1-4].
2) Расчет эритроцитарных индексов также дает направление для диагностического поиска [1-4]:
- Цветовой показатель (норма 0,86-1,05). Гипохромия по результатам анализа может свидетельствовать в пользу железодефицитной анемии, гиперхромия – В12-фолиево-дефицитной анемии.
- MCV – средний объем эритроцитов (80-100 фл). Микроцитоз может быть симптомом железодефицита, макроцитоз – В12-фолиево-дефицитной анемии, нормоцитоз возможен при хронических анемиях.
- MCH – содержание гемоглобина в эритроците (28-32 пг)
- MCHC – средняя концентрация гемоглобина в эритроците (300-308 г/л)
- RDW (red blood cell distribution width) – вариабельность размеров эритроцитов в общей циркулирующей популяции клеток (11,5-14.5%)
3) В зависимости от сформировавшихся подозрений врача, пациенту назначаются те или иные дополнительные биохимические исследования крови, включающие:
- Сывороточное железо
- Ферритин
- ОЖСС
- НТЖ
- ЛДГ
- Гаптоглобин
- АЛТ
- АСТ
- Общ. билирубин: прямой и непрямой
- Общий белок
- Свободный гемоглобин
- Витамин В12
- Фолиевая кислота
- Эритропоэтин в сыворотке
- Ферритин и протопорфирин в эритроцитах
- Метилмалонова кислота и уробилиноген в моче
- Стекобелин в кале
Эти показатели, в целом, позволяют провести дифференциальную диагностику между железодефицитной, В12-фолиево-дефицитной, гемолитической и апластической анемией. Сергей Геннадьевич подчеркнул, что не следует каждому пациенту с анемией назначать полный список анализов. После оценки общего анализа крови у врача, как правило, уже формируется представление о предварительном диагнозе, и оценка конкретных единичных показателей, по сути, необходима для подтверждения уже имеющихся подозрений [1-4].
Анемией страдает примерно четверть населения планеты, и причиной половины из этих анемий является дефицит железа [5]. Профилактика и лечение дефицита железа является основной целью общественного здравоохранения, особенно среди женщин, детей и отдельных лиц в странах с низким уровнем дохода [5]. Распространенность железодефицитной анемии (ЖДА) в РФ среди гинекологических пациенток составляет около 40%, а распространенность дефицита железа (анемия + латентный дефицит) достигает 100%, что не может не беспокоить, поскольку доказано, что дефицит железа увеличивает риск материнской и младенческой смертности, инфекционной заболеваемости, снижения репродуктивной функции, работоспособности и качества жизни и т.д. [6-8]. Таким образом, ЖДА представляет собой не только медицинскую, но и крупную социальную проблему.
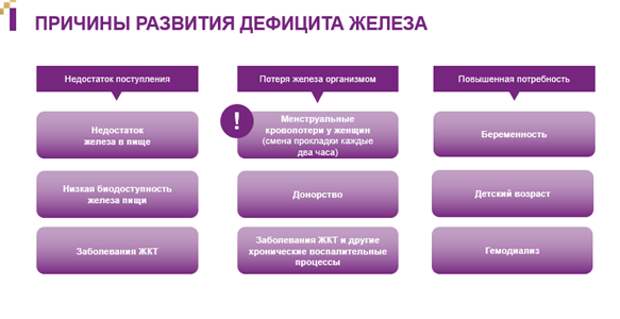
Железо в организме человека является важнейшим элементом транспорта кислорода и клеточного дыхания, играет определенную роль в синтезе ДНК, росте клеток и иммунной защите, вовлечено в процессы активации и ингибирования целого ряда ферментов [9, 10]. Содержание железа в организме регулируется контролируемой абсорбцией таким образом, что недостаток микроэлемента приводит к повышению его всасывания в двенадцатиперстной кишке и начальных отделах тощей кишки (и в меньшей степени – в дистальных отделах тощей кишки) [11].
Основной проблемой профилактики железодефицита является тот факт, что недостаток железа невозможно устранить только с помощью диеты [12, 13]. Грамотное сбалансированное питание позволяет лишь покрыть физиологическую потребность организма в железе, но не устранить его дефицит [12, 13]. Для поддержания нормального уровня железа или для профилактики прогрессирования железодефицита в пищевом рационе следует предусмотреть употребление продуктов с относительно высоким содержанием гемового железа и продукты, полученные путем естественной ферментации, которые улучшают его всасывание. Крайне важно объяснить пациенту, что избыточное потребление чая, кофе, красного вина, какао, цветных бобов, цельнозерновых злаков и кальцийсодержащих (молочных) продуктов, а также антацидов, подавляет всасывание железа и может приводить к развитию его дефицита [12, 13]. Приемом этих продуктов также может объясняться отсутствие эффективности назначенной пероральной терапии ЖДА, поэтому на контрольных визитах необходимо общаться с пациентом, проясняя особенности его питания и информируя об особенностях метаболизма железа.
При назначении диеты и/или терапии железодефицита следует учитывать, что при приеме внутрь железо всегда окисляется до Fе3+, а через транспортер 2х-валентных металлов в кишечнике всасываются только 2х-валентные ионы [14]. Аскорбиновая кислота предотвращает преобразование двухвалентного в трехвалентное железо, тем самым способствуя его всасыванию [14]. Совместное применение железосодержащих препаратов с аскорбиновой кислотой улучшает всасывание железа в несколько раз.
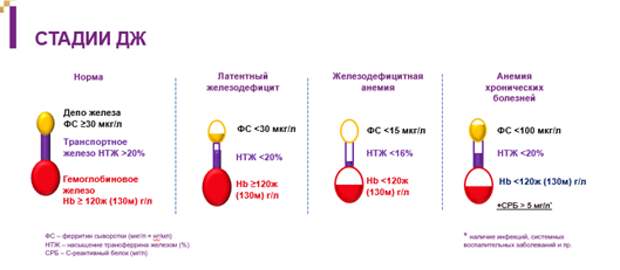
В диагностике ЖДА наиболее чувствительным и специфичным показателем является сывороточный ферритин [15, 16]. Его снижение ниже 30 мкг/л свидетельствует об абсолютном дефиците железа. Однако важно учитывать, что при наличии воспаления (СРБ > 5 мг/л) и/или НТЖ (насыщение трансферрина железом) <20%, показателем дефицита железа является сывороточный ферритин <100 мкг/л [15, 16]. Развитию ЖДА предшествует период латентного железодефицита (ЛДЖ), лабораторными критериями которого служат низкие показатели сывороточного железа и ферритина на фоне нормального уровня гемоглобина [17].
В 2024 г в России вышли новые Клинические рекомендации по ведению пациентов с ЖДА [17]. Согласно новой версии рекомендаций, в группы риска по данному заболеванию входят пациенты с обильной кровопотерей менструальной или иной природы; потребляющие железо в недостаточном количестве; а также больные, уже имевшие диагноз ЖДА (по сути, с недолеченным ранее железодефицитом). В целом, новый документ подтверждает ключевые подходы к диагностике железодефицита [17]:
- Пациентам с анемическим синдромом рекомендуется выполнение общего клинического анализа крови, оценка гематокрита, исследование уровня эритроцитов и ретикулоцитов с определением среднего содержания и средней концентрации гемоглобина в эритроцитах, определение размеров эритроцитов.
- При подозрении на ЖДА рекомендуется исследовать сывороточные показатели обмена железа: уровни ферритина, трансферрина, железосвязывающей способности сыворотки (ОЖСС), железа сыворотки крови, коэффициент насыщения трансферрина железом (НТЖ).
- Степень анемии определяется по уровню гемоглобина: 119-90 г/л – анемия легкой степени, 89-70 г/л – анемия средней степени, 69 и ниже г/л – анемия тяжелой степени, являющаяся показанием к госпитализации.
- Необходимо проводить дифференциальную диагностику ЖДА и ЛДЖ. При ЛДЖ уровень гемоглобина остается нормальным, но другие показатели, такие как MCV и MCH (микроцитоз, гипохормия), и уровень ферритина сыворотки крови могут указывать на наличие начальной стадии заболевания, которая также нуждается в терапии.
- При постановке диагноза необходимо указать степень тяжести дефицита железа, степень тяжести анемии, степень выраженности симптомов анемии и причину ее развития. (Пример: Железодефицитная анемия. Анемия тяжелой степени без клинических проявлений на фоне состоявшегося желудочно-кишечного кровотечения D50.0).
- Распространенность ЖДА требует принятие обширных профилактических мер. Скрининг для выявления анемии проводят у всех небеременных женщин каждые 5–10 лет в течение всего детородного возраста. Ежегодному скринингу подлежат женщины с факторами риска развития ЖДА. Прием препаратов железа с профилактической целью предназначен для лиц из групп риска [17].
Первой линией терапии ЖДА (легкой и средней тяжести) и ЛДЖ являются пероральные препараты двухвалентного и трехвалентного железа [17]. При этом, дозы препаратов железа и длительность лечения рассчитывают индивидуально с учетом возраста, массы тела пациента и терапевтического плана лечения [17]. В соответствии с рекомендацией ВОЗ, оптимальная доза железа для лечения ЖДА составляет 120 мг в день. Терапия дефицита железа должна проводиться до восполнения уровня тканевых запасов железа (повышение ферритина более 40-60 нг/мл) и регресса проявлений сидеропенического синдрома [17]. Беременным с ЖДА легкой и средней степени тяжести или с ЛДЖ, для предотвращения увеличения перинатальных рисков и дефицита железа у младенца, рекомендуется назначать (на первом и втором триместре) пероральные препараты двух- или трехвалентного железа в дозе от 60 до 100 мг элементарного железа в день [17]. После нормализации концентрации Hb следует продолжить прием препаратов, по крайней мере, в течение трех месяцев для восполнения запасов железа в организме [17]. В случае послеродовой анемии легкой и средней степени тяжести при стабильной гемодинамике, отсутствии или слабой выраженности симптомов анемии, назначаются пероральные препараты железа (в расчете от 40 до 100 мг элементарного железа в день) ежедневно в течение трех месяцев.
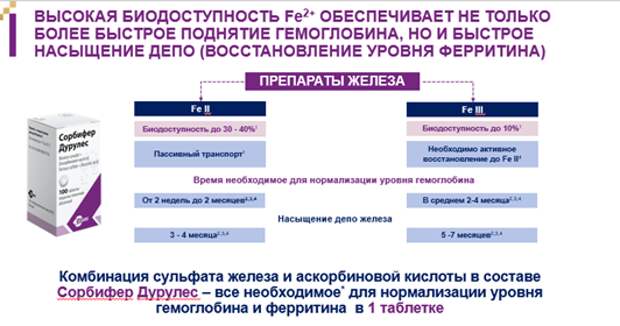
При выборе конкретного препарата необходимо учитывать, что биодоступность средств, содержащих Fe2+, в 3 раза выше, чем содержащих Fe3+ [18-21]. В кишечнике всасываются только двухвалентные ионы железа, поэтому если препарат содержит Fe3+, его приходится восстанавливать до Fe2+, например, с помощью витамина С или медьзависимой ферроредуктазы на мембране энтероцитов [18, 19]. Доктор Захаров отметил необходимость тщательно изучать инструкции к назначаемым железосодержащим препаратам на предмет не только количества, но и качества содержащегося в нем железа, поскольку содержание необходимой дозы в препарате не означает, что она полностью сможет абсорбироваться в организме. Эффективность препаратов двухвалентного железа в сочетании с аскорбиновой кислотой в 4 раза выше по сравнению с препаратами трехвалентного железа без нее [18-21]. По мнению спикера, оптимальным препаратом для терапии ЖДА и ЛДЖ, в том числе у беременных, является Сорбифер Дурулес, содержащий комбинацию сульфата железа и аскорбиновой кислоты [22].
Сравнение форм доставки железа показывает, что пероральные препараты в виде таблеток являются наиболее удобной и безопасной формой профилактики и терапии дефицита железа [17, 23]. Так, жидкие формы перорального приема, по сравнению с таблетками, предполагают усиленный контакт слизистой с железом, что, с одной стороны, увеличивает всасывание, но с другой, повышает количество нежелательных явлений (привкус во рту, потемнение эмали зубов, повышение числа побочных эффектов при заболеваниях желудка). Кроме того, они неудобны в использовании (необходимо разводить, открывать или ломать ампулу и т. д.), и часто не сочетается с вождением транспорта [17, 23]. Инъекционные препараты являются второй линией терапии и назначаются только при доказанном абсолютном дефиците железа, при тяжелой анемии, требующей госпитализации, и только в стационаре [17]. Использование внутримышечных инъекционных препаратов железа часто сопряжено с образованием инъекционных абсцессов. Использование внутривенного введения препаратов железа рекомендуется при тяжелой ЖДА (концентрация гемоглобина менее 70 г/л), продолжающейся кровопотере, а также в случаях неэффективности, плохой переносимости или наличия противопоказаний к применению препаратов железа в лекарственной форме для перорального применения для достижения излечения [17]. Парентеральные препараты можно применять при необходимости быстро поднять гемоглобин, например перед операцией, однако, по мнению спикера, в таких случаях стоит тщательно оценить соотношение пользы и рисков инъекционной терапии железодефицита, и по возможности выбрать более безопасную пероральную форму. Важно отметить также, что БАДы для лечения железодефицитных анемий и состояний, связанных с дефицитом железа, не показаны [17].
Таким образом, препаратами выбора для профилактики и лечения ЖДА и ЛЖД являются средства, содержащие:
- двухвалентное железо;
- аскорбиновую кислоту, увеличивающую всасывание железа на 30%;
- максимально эффективную разовую дозу в 100 мг элементарного железа, при которой всасывается до 14 мг металла.
Кроме того, препараты с замедленным высвобождением позволяют увеличить всасывание и снизить побочные эффекты.
Примером такого препарата, по мнению спикера, является Сорбифер Дурулес. В своей клинической практике Сергей Геннадьевич уже более 15 лет активно рекомендует этот препарат, и особенно часто – пациентам с плохой приверженностью жидким формам терапии ЖДА. В 1 таблетке Сорбифер Дурулес содержится сульфат железа в количестве 100 мг элементарного 2-х валентного железа, что соответствует дозе, рекомендованной Клиническими рекомендациями. Комбинация с 60 мг аскорбиновой кислоты улучшает процесс всасывания ионов железа, а технология замедленного высвобождения ионов железа (в течение 6 часов) позволяет избегать пиковых нагрузок на слизистую кишечника и способствует хорошей переносимости препарата [22]. За последние 10 лет препаратом Сорбифер Дурулес в 10 странах было пролечено 11 млн пациентов [24]. Он занимает первое место в категории препаратов железа по доле рынка и выписке, и является победителем премии Russian Pharma Awards 2022 в номинации «Лечение анемии у беременных и кормящих» [25, 26].

Согласно результатам клинических исследований, Сорбифер Дурулес обеспечивал достоверное повышение гемоглобина уже через 2 недели лечения и полное восстановление его уровня до 140 г/л на 5й неделе [27]. Благодаря технологии замедленного высвобождения «Дурулес», терапия хорошо переносится в 95% случаев [28]. Спикер отметил, что следование простым рекомендациям по приему препарата – не делить и не разжевывать таблетку, и запивать ее достаточным количеством воды, – позволит подавляющему большинству пациентов избежать побочных эффектов.
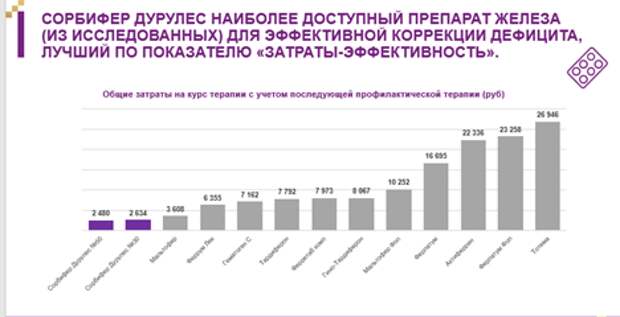
Интересно также, что Сорбифер Дурулес является на сегодняшний день наиболее доступным препаратом для эффективной коррекции дефицита железа [29]. В исследовании клинико-экономических параметров терапии дефицита железа с применением различных железосодержащих препаратов, наименее затратным и наиболее эффективным на курс лечения (наилучший показатель «затраты-эффективность») показал себя препарат Сорбифер Дурулес № 50 (2 480 руб), наиболее затратными – Феррум Лек для инъекций в ампулах (33 228 руб) и Тотема для перорального приема в ампулах (26 946 руб) [29].
Железодефицитная анемия бесспорно является наиболее распространенной формой анемий. Однако на приеме у врача, вне зависимости от его специальности, могут появиться пациенты не только с ЖДА, но и другими видами анемий: анемией на фоне хронического заболевания, B12-фолиево-дефицитной, мегалобластной, сидеробластной апластической, гемолитической анемией и др., каждая из которых отличается своей лабораторной картиной. Чтобы не упустить начало заболевания и предотвратить его переход в тяжелую форму, необходимо уделять пристальное внимание показателям анализа крови, а при наличии сомнений – направлять пациента на консультацию к гематологу.
Литература:
- Анемии: краткое руководство для врачей всех специальностей / Под ред. О.А. Рукавицына. 2-е изд., перераб. и доп. М.: ГЭОТАР-Медиа, 2021. 353 с.: ил.
- Рукавицын О.А. (ред.). Гематология: национальное руководство. М.: ГЭОТАР-Медиа, 2016. 784 с.)
- Абдурахманов Д.Т. Железодефицитная анемия при заболеваниях желудочно-кишечного тракта // Фарматека. 2012. № 13. С. 9–14.4.
- Сахин В.Т., Крюков Е.В., Рукавицын О.А. Анемия хронических заболеваний / Под. общ. ред. Е.В. Крюкова. М.: ГЭОТАР-Медиа, 2020. 160 с.
- Treatment of iron deficiency anemia in adults. https://www.uptodate.com/contents/treatment-of-iron-deficiency-anemia-in-adults?search=iron%20anemia&source=search_result&selectedTitle=1~150&usage_type=default&display_rank=1
- WHO guideline on use of ferritin concentrations to assess iron status in individuals and populations. https://www.who.int/publications-detail/9789240000124,
- Yokoi, K., & Konomi, A. (2017). British Journal of Nutrition, 117(10), 1422-1431;
- Houston B et al; BMJ Open 2018;8:e019240. doi:10.1136/ bmjopen-2017-019240 The global prevalence of anaemia in 2011. Geneva: World Health Organization; 2015.
- Wander K, Shell-Duncan B, Brindle E. Lower incidence of respiratory infections among iron-deficient children in Kilimanjaro, Tanzania. Evol Med Public Health. 2017;2017(1):109–119.
- Puig S, Ramos-Alonso L, Romero AM, Martínez-Pastor MT. The elemental role of iron in DNA synthesis and repair. Metallomics. 2017;9(11):1483–1500. Denic S, Agarwal MM. Nutritional iron deficiency: an evolutionary perspective. Nutrition. 2007;23(7-8):603–614.
- Таюпова И.М. Физиологические и биохимические аспекты дефицита железа у беременных. Евразийский Союз Ученых (ЕСУ). 2016; 30
- Струтынский А.В. Диагностика и лечение железодефицитных анемий. https://www.rmj.ru/articles/gematologiya/Diagnostika_i_lechenie_ghelezodeficitnyh_anemiy/#ixzz7PCrwqLoQ
- Гороховская Г.Н., Мартынов A.И., Юн B.Л., Петина М.М. Современный взгляд терапевта на проблему железодефицитной анемии у пациентов с сердечно-сосудистой патологией. Медицинский Совет. 2020;(14):70-78. https://doi.org/10.21518/2079-701X-2020-14-70-78
- D.J.R. Lane, D.R. Richardson / Free Radical Biology and Medicine 75 (2014) 69–83
- Iron Deficiency Anaemia Assessment, Prevention, and Control. A guide for programme managers. WHO, 2001;
- Crichton R. Danielson Bo G., Geisser P. UNI-MED Verlag AG, 2008; 3. Qunibi WY. Arzneimittelforschung 2010;60:399‒412; 4. Clark SF. Nutr Clin Pract. 2008;23:128‒141; 5. Breymann C, Huch R. UNI-MED Verlag AG, Bremen 2008; 6. Muñoz et al. Anaesthesia 2017, 72, 233-47.
- Клинические рекомендации «Железодефицитная анемия», 2024
- Стуклов Н.И. и соавт. Эффективность и переносимость препаратов железа. Что важнее? Существует ли оптимальное решение? Поликлиника 2/2014
- Стуклов Н.И., Семенова Е.Н. Железодефицитная анемия. Современная тактика диагностики и лечения. Критерии эффективности терапии // Клиническая медицина. – 2013. — № 12. — С. 61 – 68
- Lane D.J., Bae D.H., Merlot A.M. et al. Duodenal cytochrome B (DCYTB) in iron metabolism: An update on function and regulation // Nutrients. 2015. Vol. 7, № 4. Р. 2274–2296. PMID: 25835049
- Eady J.J., Wormstone Y.M., Heaton S.J. et al. Differential effects of basolateral and apical iron supply on iron transport in Caco-2 cells // Genes. Nutr. 2015. Vol. 10, № 3. Р. 463
- Инструкция по медицинскому применению ЛП Сорбифер Дурулес, РУ ЛП-N (000080)-(РГ-RU) от 08.10.2020
- Стуклов Н.И. Железодефицитная анемия в практике гинеколога. Алгоритмы диагностики, профилактики и лечения. Акушерство и гинекология. №7, 2016: 99-104
- Расчетный показатель продаж по данным IQVIA, с 2012 по 2022 гг., с учетом 2 –х месячного курса лечения по 200 мг в сутки
- IQVIA, Prindex data 2024
- Russian Pharma Awards 2022
- Дворецкий Л.И. и соавт. Сравнительная эффективность железосодержащих препаратов у больных железодефицитной анемией. Клиницист. 2007;1:1-8.
- Ю.Э. Доброхотова, А.Х. Каранашева «Антианемическая терапия у больных с субмукозной миомой матки после эмболизации маточных артерий» Лечебное дело 4,2021
- Воробьев П.А. Клинико-экономический анализ для оптимизации затрат на прием препаратов при дефиците железа / П.А. Воробьев, Е.А. Лучинин, А.П. Воробьев, Л.С. Краснова // Проблемы стандартизации в здравоохранении. 2023; 1-2:3-11. DOI: 10.26347/1607-2502202301-02003-011
Свежие комментарии