
С 19 по 21 февраля в Москве прошло главное событие в области неврологии и психиатрии – Юбилейная междисциплинарная конференция с международным участием «XX Вейновские чтения». В рамках конференции о пограничных проблемах неврологии и психиатрии, а также диагностике и терапии нейропсихиатрических расстройств на примере известных личностей и литературных персонажей рассказали эксперты симпозиума «В «сумрачном лесу» неврологии и психиатрии».
Председателем симпозиума выступил Олег Семенович Левин, д.м.н., профессор, заведующий кафедрой неврологии с курсом рефлексологии и мануальной терапии Российской медицинской академии непрерывного профессионального образования (РМАНПО), руководитель Центра экстрапирамидных заболеваний, член Международного общества по изучению расстройств движений (Movement Disorder Society) и Европейской академии неврологии (European Academy of Neurology), член панели по расстройствам движения Европейской академии неврологии, Член Правления Всероссийского общества неврологов, вице-президент Национального общества по изучению болезни Паркинсона и расстройств движений.Проблема диагностики нейропсихиатрических расстройств
Во вступительном докладе сопредседатель симпозиума Алексей Борисович Данилов, д.м.н., заведующий кафедрой нервных болезней ИПО Первого МГМУ им. И.М. Сеченова, исполнительный директор Ассоциации междисциплинарной медицины, проиллюстрировал данными статистики актуальность проблемы своевременной диагностики тревожно-депрессивных расстройств и деменции. Эксперт отметил, что сегодня от тревоги и депрессии страдает около 50% взрослого населения планеты, а к 2030 году, по оценкам ВОЗ, депрессия станет первой по распространенности причиной нетрудоспособности.
При этом только у 1 из 10 пациентов депрессия или тревога будут диагностированы своевременно. Вместе с этим неуклонно растет распространенность деменции – каждый год диагностируется 10 миллионов новых случаев, а всего в настоящее время насчитывается 55 миллионов человек с деменцией. Диагностика деменции также находится на критически низком уровне – в 2021 году в РФ диагноз был установлен только у 9% пациентов с деменцией. Отчасти эта неутешительная статистика связана с тем, что врачам непсихиатрического профиля зачастую не хватает времени приема на проведение полноценного психоневрологического обследования, а сами пациенты не всегда готовы обращаться к психиатру. В таких случаях облегчить диагностику и первичное выявление возможных психоневрологических нарушений могут помочь современные технологии, позволяющие автоматизировать процесс сбора и анализа данных и тем самым ускорить получение результатов нейропсихологического тестирования. Наиболее удобными и полезными в условиях амбулаторной практики врача первичного звена являются мобильные инструменты, включающие основные верифицированные клинические шкалы. Один из примеров – отечественное приложение Невросканнер, предназначенное для профессионального использования. Приложение включает набор шкал для диагностики вегетативных (шкала Вейна) и когнитивных нарушений (Опросник для скрининга деменции (AD8), Аризонский опросник для родственников, краткая шкала оценки психического статуса (MMSE), батарея тестов для оценки лобной дисфункции (FAB)) и тревожно-депрессивных расстройств (шкала Спилбергера-Ханина (STAI), госпитальная шкала тревоги и депрессии (HADS), шкала Монтгомери-Асберг (MADRS)). Медицинское наполнение приложения подготовлено ведущими специалистами в области неврологии и психиатрии, сотрудниками ФГБУ «Национального медицинского исследовательского центра психиатрии и неврологии им. В.М. Бехтерева» Минздрава России. Результат, полученный в приложении, может помочь дифференцировать вегетативные, когнитивные, неврологические и психиатрические расстройства, а также послужить основанием для направления пациента к профильному специалисту. Анкету можно заполнять на любом устройстве – компьютере или телефоне, а также использовать бумажную версию для заполнения от руки. Отличительной особенностью приложения является то, что помимо подробного заключения, оно предлагает варианты терапии. Преимущества и рекомендации по использованию приложения Невросканнер как современного инструмента диагностики были представлены в статье Николая Григорьевича Незнанова и Анны Владимировны Васильевой «Цифровизация в оказании помощи в области психического здоровья. Новые возможности для специалистов и пациентов», опубликованной в журнале «Национальное здравоохранение».Тревожно-депрессивные расстройства и расстройства адаптации
Продолжая дискуссию о диагностике и терапии нейропсихиатрических расстройств, Анна Владимировна Васильева, д.м.н., руководитель международного отдела, главный научный сотрудник отделения лечения пограничных психических расстройств и психотерапии ФГБУ «НМИЦ ПН им. В.М. Бехтерева» Минздрава России, профессор кафедры психотерапии, медицинской психологии и сексологии ФГБОУ ВО «Северо-Западный государственный медицинский университет им. И.И. Мечникова» Минздрава России, выступила с докладом «Первородный грех и расстройство адаптации».
«Отличительной особенностью человека как биологического вида является осознание своей смертности. В глобальном смысле именно оно и повлекло за собой развитие тревожных расстройств, не связанных с непосредственно адаптацией к меняющимся условиям среды и выживанием, а в большей степени обусловленных с переживанием конечности жизни или потери социального статуса в обществе». – отметила эксперт.
Вместе с утратой спокойствия и комфорта, инициаторами развития расстройств адаптации служат нарушения базовых убеждений – неуязвимости, предсказуемости событий, иллюзии контроля, а также наличия всемогущего, всепонимающего, всепрощающего и бесконечно любящего другого. В литературном смысле потерю этих «райских» потребностей можно метафорично сравнить с изгнанием из рая Адама и Евы, у которых можно было бы предположить высокий уровень ситуативной тревожности. В реальном мире этот феномен наиболее ярко проявляется при миграции. Как показывают последние исследования заболеваемости психическими расстройствами у беженцев и вынужденных переселенцев, наиболее распространенными неспецифическими нарушениями у этой группы лиц являются тревожные расстройства: по данным А.И. Былим, среди обследованных им беженцев тревога выявлялась в 82.7% случаев. Дифференцировать личностную и ситуативную тревогу позволяет шкала Спилбергера-Ханина, которая в данном случае позволяет предположить преобладание ситуационной тревожности.
Первичным фактором формирования тревоги часто является интенсивное воздействие внешнего стрессора, вызывающего прорыв адаптационного барьера и развитие социально-стрессовых расстройств, о которых писал Ю.А. Александровский: «Психические расстройства не являются специфическими – они обусловлены общими механизмами развития состояния психической дезадаптации». Помимо острого стресса и дезадаптации, тревогу может вызывать неопределенность и непредсказуемость событий. Так, при фатофобии человек испытывает страх или тревогу за свою судьбу или будущее в соответствующем плане жизни. Это состояние в большинстве случаев является следствием индивидуально трудноразрешимой ситуации, из которой больные не могут найти выход. Страх за свою судьбу в биологическом плане проявляется танатофобией или страхом смерти. При этом конкретное содержание танатофобии определяется характером ведущего нейросоматического синдрома (А.Я. Страумит).
При диагностике расстройств адаптации (F43.2) критически важно определить этиологию и выделить стрессовое событие, которое инициировало развитие расстройства на фоне индивидуальной предрасположенности или уязвимости. Другими критериями диагностики расстройств адаптация являются характерные клинические проявления, в том числе наличие и преобладание депрессии, тревоги, беспокойства, неспособности справляться, планировать или продолжать оставаться в ситуации, а также снижение продуктивности в повседневных делах и нарушение сна. У подростков может отмечаться агрессивное или диссоциальное поведение.
В своей работе «О выборе психотропных препаратов для лечения расстройств адаптации у вынужденных переселенцев» Ю.А. Александровский и А.С. Аведисова утверждали, что несмотря на то, что расстройства адаптации в принципе относятся к состояниям с благоприятным прогнозом и успешно поддаются психотерапевтическому воздействию, риск развития более сложных психопатологических расстройств, например, генерализованных тревожных расстройств, патологических развитий личности и др., при длительно действующих и неразрешимых в настоящее время стрессовых ситуациях достаточно высок. Это требует проведения психофармакотерапии с использованием транквилизаторов, в наибольшей степени соответствующих критерию безопасности. Так психотерапия будет оказывать лечебное воздействие на психику, а через нее на организм пациента, а медикаментозная терапия будет проявлять синергический эффект. При этом тревога, ассоциированная с расстройствами адаптации, как правило, не требует «тяжелых» анксиолитических препаратов. В данном случае предпочтение следует отдавать анксиолитикам, оказывающим быстрый эффект, и вместе с этим влияющим не только на психические, но и соматические проявления тревоги. Из группы дневных анксиолитиков этим критериям соответствует тофизопам (Грандаксин), который действует на все «звенья» расстройств адаптации. Помимо противотревожного, Грандаксин обладает вегетокорригирующим эффектом и положительно влияет на сон, не вызывает привыкание, миорелаксацию и седацию, что позволяет пациентам вести активный образ жизни. Ключевым преимуществом препарата является быстрый эффект: у пациентов, принимающих тофизопам в дозе 2 таблетки в сутки в течение двух недель, наблюдалось более чем двукратное уменьшение тревожного состояния, нарушений сна и соматических проявлений тревоги. В силу хорошей переносимости и умеренной стимулирующей активности лечение можно начинать сразу с необходимой дозы (1-2 таблетки от 1 до 3 раз в день, максимальная суточная доза – 300 мг). Для купирования острых эпизодов тревоги Грандаксин можно принимать нерегулярно по 1-2 таблетки.
О тревожных расстройствах в контексте гендерных особенностей рассказала Елена Евгеньевна Васенина, д.м.н., доцент кафедры неврологии с курсом рефлексологии и мануальной терапии ФГБОУ ДПО РМАНПО, в докладе «Тревога в гендерных зеркалах». В качестве художественной иллюстрации «клинического примера» эксперт продемонстрировала ролик о Людмиле Прокофьевне из фильма «Служебный роман» и попросила слушателей оценить уровень тревоги (отсутствие тревоги; субклиническая выраженная; клиническая выраженная) и депрессии (отсутствие депрессии; субклиническая выраженная; клиническая выраженная).
Главная героиня – незамужняя женщина в возрасте 36 лет, предпочитает находиться в одиночестве, имеет относительно узкий круг творческих интересов, вредные привычки отрицает. Героиня иногда отмечает эпизоды плаксивости и повышенной эмоциональности (хотя чаще всего сдерживает свои эмоции), отсутствие радости и удовольствия, страхи, которые «компенсирует» работой.
Для определения уровня тревоги и депрессии у героини фильма Елена Евгеньева заполнила опросник Госпитальной шкалы тревоги и депрессии (HADS) в приложении Невросканнер. Результат показал наличие клинической тревоги (11 баллов) и депрессии (12 баллов). Ключевыми симптомами, подтверждающими диагноз, были высокая степень тревожности пациентки («уничтожила» всех подруг, переживания по поводу «Министра», несмотря на эмоциональный стрессовый эпизод), трудоголизм и перфекционизм. Такие проявления тревоги характерны именно для женского пола.
В целом, среди женщин тревожные расстройства встречаются в 2.5 раза чаще, и у них также достоверно выше риск развития депрессии. Депрессия и тревога у женщин характеризуются более длительным течением, тяжелыми проявлениями и склонностью к рецидивам. Вместе с этим клинический «ответ» на терапию лучше у мужчин: у них наблюдается более быстрое купирование эпизода и более стабильное дальнейшее течение. Эти данные позволяют предположить роль половых гормонов в определении гендерной специфичности риска развития, течения и проявления тревожных расстройств.
Известно, что мужские половые гормоны «защищают» от развития аффективных нарушений, в то время как женские половые гормоны, наоборот, «предрасполагают» к их развитию. В подтверждение роли тестостерона как «протективного» фактора в развитии тревоги свидетельствуют данные, которые показывают, что мужчины с гипогонадизмом значительно чаще страдают различными вариантами аффективных нарушений, а применение андроген-подавляющей терапии в лечении рака предстательной железы увеличивает риск развития расстройств тревожного спектра. Кроме того, у женщин с диагностированными тревожными расстройствами отмечена обратная корреляционная связь риска развития тревоги с уровнем тестостерона (чем ниже показатели, тем выше риск), а заместительная терапия тестостероном способствовала купированию тревоги как у мужчин, так и у женщин. Таким образом, более низкий физиологический уровень тестостерона (в 10 раз) у женщин, а также его возрастное снижение отчасти объясняют большую «предрасположенность» женского пола к расстройствам тревожного спектра.
Каким образом тестостерон может влиять на «предрасположенность» к тревожным расстройствам? На нейрональном уровне, у женщин под воздействием половых гормонов более активно, в сравнении с мужчинами, развивается преоптическая область гипоталамуса – ключевая «зона» материнского инстинкта. У мужчин более активно развивается прилежащее ядро – центр системы вознаграждения или системы внутреннего подкрепления, которая представляет собой совокупность структур нервной системы, участвующих в регулировании и контроле целенаправленного поведения на основании положительных эмоций и действий. Ключевым нейромедиатором этой системы является дофамин, истинный «гормон удовольствия».
Действия, поступки и решения «закрепляются» положительными эмоциями: если результат приносит удовольствие и «пользу», то поведение и цель «встраиваются» в автобиографическую память.
Эволюционная «андрогенность» удовольствия, вероятно, и определила большую склонность женщин к расстройствам тревожного спектра. В частности, выброс дофамина и активность «системы вознаграждения» зависят от уровня тестостерона и меняется в течение жизни. По всей видимости, именно эволюционно «базовые» мужские функции, но не женские роли, и ориентированы на систему вознаграждения. Так, женщины в своем поведении менее ориентированы на достижение результата с целью получения удовольствия и положительных эмоций, а их действия в большей степени определяются не непосредственным получением вознаграждения, а социальными нормами, самоопределением и другими «когнитивными» мотивациями. Этим в том числе объясняется более высокий уровень и частота перфекционизма и неудовлетворенности своими результатами у женщин. Таким образом, женщины в своих действиях и поведении физиологически менее ориентированы на положительные эмоции, труднее получают удовольствие «от момента» и достижения результата и не умеют останавливаться, если что-то не приносит положительного подкрепления. Это и определяет меньшую толерантность женщин к стрессу и более высокий риск тревожных расстройств. На физиологическом уровне дополнительными факторами «женского» лица тревоги являются конечные метаболиты тестостерона (андростан-диолы), которые имеют сродство к ГАМК-ергическим рецепторам. Выступая в роли нейромодуляторов, они снижают активность миндалины, а вместе с этим и выраженность стрессового ответа. Именно поэтому женщины более склонны к затяжным «реактивным» стрессовым ответам.
Ключевым нейрональным механизмом большинства расстройств тревожного спектра, независимо от пола, является нарушение взаимосвязи и координированной работы между структурами лимбической системы, которая обеспечивает стрессовый рефлекторный ответ, и префронтальной коры (в частности, префронтальной коры неокортекса), участвующей в когнитивной обработке стрессового эпизода. Вместе с этим важную роль в определении целей воздействия и стратегии терапии также играет и понимание физиологических основ гендерных различий в предрасположенности и течении тревожных расстройств. Для непосредственного подавления стрессового ответа, который реализуется за счет активности миндалины, используются анксиолитики. Для купирования стресс-ассоциированной тревоги подходят как анксиолитики бензодиазепинового ряда, имеющие сродство к ГАМК-ергическим рецепторам миндалины (например, дневной анксиолитик тофизопам), так и атипичные небензодиазепиновые анксиолитики, обладающие сродством к дофаминергическим и серотонинергическим рецепторам. Последние способны не только купировать тревогу, но и оказывать действие на систему вознаграждения, что позволяет применять их как для лечения тревоги, так и в составе комбинированной терапии депрессии. Например, атипичный анксиолитик буспирон (Спитомин) действует как частичный агонист постсинаптических и полный агонист пресинаптических 5HT-1A серотониновых рецепторов, а также агонист D2 дофаминовых рецепторов, что обуславливает его антидепрессивный и противотревожный эффекты, включая коррекцию вегетативной дисфункции, моторного напряжения, апатии и нарушений сна. За счет стимуляции системы вознаграждения буспирон также оказывает просексуальное действие, способен уменьшать зависимость, повышать концентрацию внимания, точность и плавность движений. Терапевтический эффект буспирона развивается постепенно и отмечается через 7-14 дней от начала лечения, поэтому лечение следует начинать с дозы 15 мг и постепенно повышать до 20 мг на 3-4 дни, до 25 мг на 5-6 дни и до 30 мг после 7-8 дней терапии (максимальная суточная доза – 60 мг). Воздействовать на механизм когнитивного контроля, т.е. обработку стрессового эпизода, позволяют антидепрессанты группы СИОЗС/СИОЗСН.
Тему тревожных и депрессивных расстройств на примере персонажей из народного фольклора продолжила Нина Владимировна Латышева, д.м.н., профессор кафедры нервных болезней ИПО ПМГМУ им. И.М. Сеченова, невролог Клиники головной боли и вегетативных расстройств академика А. Вейна, в своем докладе «Печаль в русских народных сказках». В качестве художественной иллюстрации депрессии на фоне хронического болевого синдрома эксперт выбрала Бабу Ягу.
С одной стороны, у Бабы Яги злобный характер: колдунья часто ворчит и ругается, насылает ненастную погоду, крадет малых детей и губит заблудившихся путников, не упускает возможности полакомиться людьми. При этом она выспрашивает героя, от нее он получает коня, богатые дары и т.д. Можно ли сказать, что Баба Яга – добрая?
Нина Владимировна попросила участников симпозиума оценить вероятный уровень депрессии у этого персонажа. Если оценивать состояние «пациентки» в приложении Невросканнер с использованием шкалы Монтгомери-Асберг (MADRS), то в кратком заключении будет указано: «Умеренная депрессия, рекомендована консультация психотерапевта или психиатра» (26 баллов). На верность диагноза указывает нарушение социального функционирования, изменения эмоционального фона и т.д. Если при дальнейшем обследовании была бы выявлена умеренная депрессия в сочетании с хроническим болевым синдромом (Баба Яга Костяная Нога – вероятный корешковый синдром?), возможными диагнозами по МКБ-10 были бы:
F32.1 – Депрессивный эпизод средней степени, который может протекать как с соматическими симптомами, так и без.
F33.1 – Рекуррентное депрессивное расстройство, текущий эпизод средней степени.
Пациенты с хронической болью могут проявлять симптомы депрессии и отличаются повышенной раздражительностью, что подталкивает неврологов к решению о проведении блокады, которая зачастую оказывается неэффективной. Насколько в таком случае вероятно, что боль – результат депрессии, а не наоборот, депрессия – это следствие болевого синдрома? Чтобы это понять, согласно МКБ-11, необходимо выявить пять из следующих десяти симптомов:
- Снижение настроения.
- Снижение чувства радости.
- Снижение концентрации внимания, сложности в принятии решения.
- Низкая самооценка или чувство вины.
- Чувство безнадежности по отношению к будущему.
- Мысли о смерти или суицидальные мысли.
- Значительное нарушение или избыток сна.
- Значительное изменение аппетита или веса.
- Психомоторное возбуждение или заторможенность.
- Усталость/снижение энергии.
Симптомы №1, 2, 8, 9, 10 присутствовали у героини сказки.
В основе хронизации боли лежат различные факторы – биофизические, генетические, психологические, социальные, а также наличие коморбидной патологии (Рис.1).
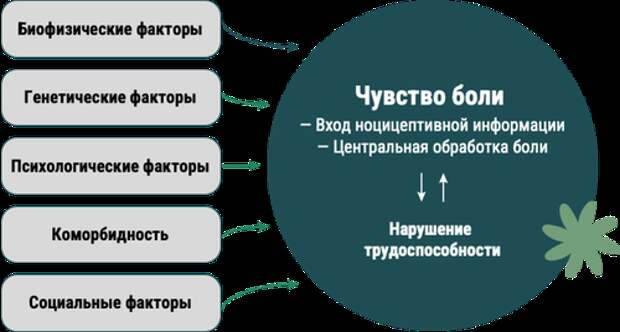
Рисунок 1. Основные факторы хронизации боли.
Однако ключевым механизмом хронизации боли в спине является центральная сенситизация, т.е. нарушение баланса между «входом» ноцицептивной информации и ее обработкой в головном мозге. Центральная сенситизация или гипервозбудимость развивается вследствие нарушения периферической сенситизации при повреждении тканей или хроническом воспалении и приводит к ремоделированию нейрональных связей в мозге (Рис. 2).
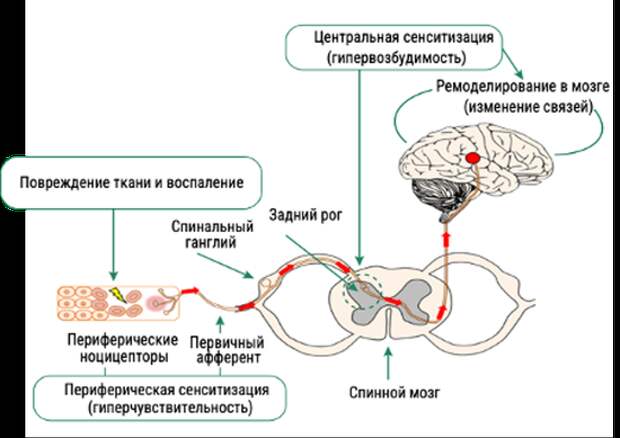
Рисунок 2. Механизм центральной и периферической сенситизации.
При хронизации боли в спине периферические факторы, включая миофасциальный болевой синдром, мышечно-тонический синдром, фасеточный синдром и радикулопатия, теряют значение. Другими словами, хроническая боль – это болезнь мозга, т.е. дезадаптивная перестройка в системах генерации и контроля боли в головном мозге (именно поэтому «погреть свои косточки» не работает при ноципластической боли). В частности, нарушение нисходящего контроля боли развивается на фоне депрессии, тревоги, катастрофизации и дезадаптивных когнитивных установок
Периферические механизмы играют ограниченную роль и только в начале заболевания. Депрессия, коморбидная боль, соматизация, зависимость и длительный анамнез боли в спине свидетельствуют о высокой вероятности центральной сенситизации и бессмысленности методов лечения «на периферии» (Рис. 3).
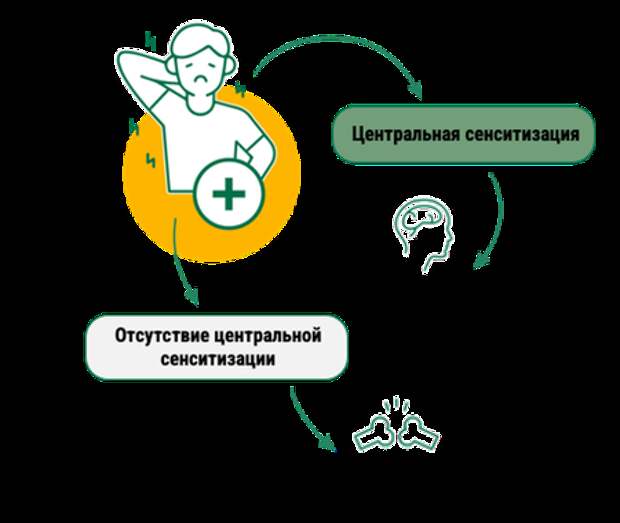
Рисунок 3. Алгоритм терапии хронической боли при наличии и отсутствии центральной сенситизации.
В таком случае лечение хронической боли должно быть основано на комплексном подходе, включающем, в первую очередь, оценку коморбидности и степени нарушения трудоспособности, и также комбинацию нелекарственных методов, направленных на снижение центральной сенситизации (обучение, психотерапия, в том числе когнитивно-поведенческая терапия, гимнастика), и фармакотерапии, в частности назначения антидепрессантов. Из антидепрессантов препаратами выбора являются серотонинергические + норадренергические препараты, например, венлафаксин (75 мг при отсутствии депрессии и 150-225 мг при наличии депрессии), дулоксетин (60-120 мг); также допускается комбинация амитриптилина и СИОЗС и, при резистентной боли можно использовать оланзапин (5 мг).
Преимуществом амитриптилина является его высокая эффективность (около 70%), способность снижать частоту любой боли, а также противотревожный эффект и положительное влияние на сон. Тем не менее 17% пациентов не переносят лечение амитриптилином, а дозу невозможно повышать до антидепрессантной. Помимо этого, препарат имеет довольно широкий спектр противопоказаний и может повышать вес. Наиболее частыми побочными эффектами являются сонливость, запор и сухость во рту. В отличие от амитриптилина венлафаксин (Велаксин) обладает антидепрессантным действием в терапевтическом диапазоне и также способен снижать частоту боли и купировать коморбидные тревожные расстройства, однако его противотревожное действие является отсроченным. Переносимость и профиль безопасности у венлафаксина лучше, чем у трициклических антидепрессантов (хотя в начале приема препарат может вызывать тошноту). Ассоциированные с приемом венлафаксина нарушения сна могут корректироваться тразодоном. Велаксин в форме капсул решает вопрос равномерности концентрации препарата в крови и дает возможность однократного приема. Целевая доза венлафаксина – 150-225 мг. Терапию следует начинать с таблетированной формы по 1/2 таблетки 37.5 мг 2 раза в день и далее наращивать дозу до 37.5 мг утром и 37.5 мг вечером (суточная доза 75 мг). При достижении суточной дозы в 75 мг можно переходить на прием капсул (1 капсула 75 мг в день в любое время). Отличительной особенностью венлафаксина является его мультимодальное действие: в дозе 75 мг препарат действует как СИОЗС и оказывает противоболевое действие; в дозе 150 мг – действует как СИОЗСН и проявляет противоболевой, антидепрессивный и противотревожный эффекты; в дозе от 225 мг и выше венлафаксин действует как СИОЗСН и модулятор дофаминергической передачи, дополнительно регулируя механизмы развития ангедонии.
Когнитивные нарушения, деменция и болезнь Альцгеймера
Продолжая тему нейропсихиатрического континуума, Николай Григорьевич Незнанов, сопредседатель симпозиума, д.м.н., заслуженный деятель науки РФ, директор ФГБУ «НМИЦ ПН им. В.М. Бехтерева» Минздрава России, Президент Российского общества психиатров, главный внештатный специалист-эксперт по психиатрии Росздравнадзора, Президент Всемирной ассоциации динамической психиатрии (World Association for Dynamic Psychiatry), заведующий кафедрой психиатрии и наркологии с курсами медицинской психологии и психосоматической медицины Первого Санкт-Петербургского государственного медицинского университета им. академика И.П. Павлова, посвятил свой доклад «Эволюция личности и семейных отношений на фоне деменции» проблеме диагностики и ведения пациентов с когнитивными нарушениями при деменции. Далее тему нейродегенеративных заболеваний раскрыл Игорь Владимирович Колыхалов, д.м.н., главный научный сотрудник ФГБНУ «Научный центр психического здоровья» РАМН, в докладе «Терапия болезни Альцгеймера: 100 лет неизвестности».
По оценкам Alzheimer's Disease International, 75% людей с деменцией во всем мире не получают корректный диагноз, при этом считается, что в некоторых странах с низким и средним уровнем дохода этот показатель достигает 90%. Наиболее распространенной формой деменции, на которую приходится от 50 до 75% всех случаев, является болезнь Альцгеймера. Сосудистая деменция – это вторая по распространенности форма деменции, на которую приходится примерно 17–30% всех случаев. На деменцию с тельцами Леви приходится примерно 10-15% всех деменций. В России среди 32 400 000 пожилых людей и 7 198 708 пациентов с цереброваскулярными заболеваниями деменцией страдают 1 744 000, и 52 251 из них имеют болезнь Альцгеймера.
Болезнь Альцгеймера впервые была описана в 1906 году немецким психиатром Алоисом Альцгеймером. Она характеризуется утратой нейронов и синапсов, образованием нейрофибриллярных клубочков и сенильных бляшек, а также атрофией различных структур головного мозга.
Актуальность вопроса ранней диагностики когнитивных нарушений у пожилых пациентов Николай Григорьевич Незнанов проиллюстрировал на примере фильма «Отец» (The Father, 2020 г.). В частности, главный актер фильма демонстрировал ряд клинических проявлений деменции (наиболее подходящий диагноз – F03 – Деменция неуточненная или F00.1 – Деменция при болезни Альцгеймера с поздним началом), которые часто упускаются из внимания при обследовании амбулаторного пациента. Одним их таких характерных проявлений были изменения личности. В литературе прошлых лет они классифицировались как старческая псевдопсихопатия. У таких пациентов могут наблюдаться сужение кругозора и интересов, утрата прежних связей с окружающим миром и аффективной отзывчивости, шаблонность взглядов и высказываний, нарастание эгоцентричности, скупость и черствость, подозрительность и придирчивость, а также злобность и бестактность. Далее в результате снижения критики подозрительность и упрямство все более сочетаются с легковерностью и внушаемостью: больные легко поддаются чужому влиянию, нередко во вред своим интересам. К психопатоподобным изменениям присоединяются признаки регресса личности, исчезают стыдливость и более тонкие нравственные установки. Помимо изменений личности у пациента в фильме наблюдались конфабуляции (ложные воспоминания или вымысел/видоизменение фактов) и конфабуляторный бред, а также экмнезия (перенесение в памяти событий прошлой жизни в настоящее; характерное проявление – неспособность узнавать себя в зеркале).
Многие из перечисленных симптомов, в частности эмоциональные и ранние поведенческие проявления деменции, не удается выявить в рамках единичного амбулаторного приема. Кроме того, зачастую пациенты обращаются к профильному специалисту (например, неврологу), уже на этапе прогрессирующих нарушений (агнозия, апраксия и др.), когда снижение когнитивных функций становится заметным и начинает мешать нормальному ежедневному функционированию, то есть на прогрессирующих стадиях, на которых терапия оказывается малоэффективной.
По мере прогрессирования когнитивных нарушений происходит ослабоумливание: сначала утрачиваются свежий опыт (наиболее поздно приобретенный и менее закрепленный материал), дольше и лучше сохраняется раньше приобретенный и прочнее закрепленный опыт. Распад психики распространяется от более сложного и дифференцированного к более простому и автоматизированному. Прежде всего страдают наиболее сложные и индивидуальные, творческие и критические, абстрагирующие и интегрирующие виды психической деятельности, в то время как старый словарный запас и способность оперировать определенным кругом установившихся понятий и представлений сохраняются относительно дольше, хотя в целом уровень суждений и умозаключений продолжает неуклонно снижаться. Параллельно происходит нарастание грубых расстройств памяти, особенно рано и глубоко нарушается запоминание, утрачивается способность к приобретению нового опыта. На прогрессирующих стадиях деменции развиваются фиксационная амнезия и амнестическая дезориентировка (утрата ориентировки в окружающей обстановке, во времени, последовательности событий и, наконец, в собственной личности). Материалы памяти и запас ранее приобретенных знаний постепенно разрушаются и опустошаются в последовательности, противоположной очередности приобретения знаний и опыта (как бы сверху, слой за слоем). В конечном итоге у больных полностью пропадает запас школьных, профессиональных и других приобретенных знаний. Одновременно у пациентов нарастают и расстройства чувственного познания окружающего мира (все виды восприятия становятся все более нечеткими и дефектными, утрачивается способность к их интеграции), а вместо адекватного узнавания окружающей обстановки и лиц происходит ложно узнавание, отражающее жизнь больных в отдаленном прошлом. Наконец, сдвиг окружающей обстановки в прошлое распространяется и на самосознание: больные считают себя детьми, молодыми людьми, окруженными родителями и другими давно умершими родственниками. При этом наблюдаются явные конфабуляции (хотя конфабуляции, относящиеся к давнему прошлому, т.е. экмнестические, при старческом слабоумии, как правило, бедны). Иногда больной перестает узнавать себя в зеркале. В процессе распада психической деятельности возникает так называемый старческий делирий (точнее – псевдоделирий, так как галлюцинаторных нарушений при этом синдроме не бывает): больные с полной амнестической дезориентировкой со сдвигом ситуации в прошлое и ложными узнаваниями проявляют особую «деловитость» и развивают мнимую деятельность, отражающую их ложные представления об окружающей обстановке и собственной личности.
При обнаружении любых «подозрительных» симптомов врачу следует проводить более глубокое, комплексное обследование пациента, включающее:
- Клиническое исследование (сбор и анализ данных анамнеза, неврологический осмотр и нейропсихологическое тестирование).
- Лабораторное исследование (общие анализы крови и мочи, биохимические исследования крови, системы гемостаза и липидного спектра, анализ на гормоны щитовидной железы, витамина В12 и фолиевой кислоты).
- Инструментальное исследование (магнитно-резонансная томография).
Для иллюстрации диагностической оценки и определения типа деменции Игорь Владимирович Колыхалов использовал художественный образ писательницы Айрис Мердок в исполнении Джуди Денч из фильма Айрис (Iris, 2001). Правдивую летопись творчества и бытия Айрис Мердок составил ее муж, профессор Джон Бэйли, описав более 40 лет их супружеской жизни, начиная со знакомства с юной оксфордской преподавательницей Айрис и заканчивая мучительной борьбой Айрис с жестокой болезнью, лишившей одаренную романистку возможности творить и жить. Согласно результатам Аризонского опросника для родственников и шкалы MMSE, заполненных в приложении Невросканнер, удалось получить заключение по возможному диагнозу пациентки – достоверно высокой вероятности деменции (21 балл) по Аризонскому опроснику и деменции умеренной степени выраженности по шале MMSE (16 баллов); оценка по шкале FAB показала, что результаты соответствуют нормальной лобной функции (16 баллов). Таким образом, наиболее вероятный диагноз героини – Деменция умеренной степени выраженности (функциональная стадия). В МКБ-10 возможными вариантами могут быть:
- G30.1 – Болезнь Альцгеймера с поздним началом
- F00.1 – Деменция при болезни Альцгеймера с поздним началом
Согласно МКБ-10, синдром деменции устанавливают на основе ряда критериев: специфичной симптоматики, степени выраженности, длительности, течении, причин и критериев исключения (Таблица 1).
Таблица 1. Критерии диагностики синдрома деменции по МКБ-10
| Симптомы | Множественный дефицит высших корковых функций,
включая нарушения памяти и, по крайней мере, одной из когнитивных функций: • речи • праксиса (исполнительной деятельности) • гнозиса (оптико-пространственной деятельности) • мышления |
| Степень выраженности | Ухудшение профессионального или социального функционирования |
| Длительность | Не менее 6 месяцев |
| Течение | Обычно хроническое или прогрессирующее |
| Причины | Церебральное заболевание или общее состояние (соматическое заболевание, интоксикация, в т.ч. медикаментозная), вторично влияющее на мозговую деятельность |
| Критерий исключения | Расстройство сознания |
Деменция характеризуется медленным прогрессированием и нарастанием когнитивных нарушений. На этапе мягких когнитивных нарушений, который длится от 1 года до 7 лет, обнаруживаются легкие субъективные/объективные нарушения памяти при нормальном функционировании. Прогрессирование деменции от мягкой до тяжелой может занимать от 1 года до 10 и более лет. На этапе мягкой деменции (19-26 баллов по шкале MMSE) развиваются легкие нарушения памяти, трудности усвоения новой информации и выполнения сложных бытовых задач, трудности ориентировки в пространстве, ограничение интересов и снижение инициативы. На стадии умеренной деменции (10-18 баллов по шкале MMSE) наблюдается прогрессирующий когнитивный дефицит, нарушение усвоения текущей информации и функционирования в быту. При тяжелой деменции (0-9 баллов по шкале MMSE) у пациента развиваются ажитация, изменение ритма сна, тотальная несостоятельность в быту и в выполнении гигиенических навыков.
Учитывая, что в пожилом возрасте редко наблюдается одна изолированная патология, трудность при диагностике может представлять и дифференциация аффективных нарушений при деменции и соматических заболеваниях и непосредственно депрессивного расстройства. В данном случае рекомендуется не ограничиваться одним методом нейропсихологической оценки, а использовать как можно больше клинических шкал. В частности, AD8 Опросник для скрининга деменции, который включает восемь вопросов с типами ответом «да»/«нет» и заполняется лицами, близкими к испытуемому, Аризонский опросник из 21 вопроса, также предназначенный для родственников больного, шкала MMSE для непосредственной оценки наличия, типа и тяжести когнитивных нарушений, и батарея тестов для оценки лобной дисфункции FAB. Упростить и ускорить сбор данных и получение результатов нейропсихологического тестирования могут помочь современные технологии, которые позволят не только выявить наличие когнитивных нарушений, но и определить степень выраженности деменции, провести дифференциальную диагностику и предложить варианты интерпретации результатов. Все эти функции сочетаются в приложении Невросканнер.
После получения результатов нейропсихологического тестирования для дальнейшей оценки состояния пациента рекомендуется консультация невролога или психиатра. При этом при осмотре и опросе должно быть диагностировано клинически значимое когнитивное снижение по сравнению с исходным уровнем, соответствующее синдрому деменции. Клинические проявления деменции должны наблюдаться отчетливо на протяжении не менее 6 месяцев: если период с начала манифестации короче, то диагноз может быть лишь предположительным. Наконец, у пациента должны отсутствовать помрачения сознания на протяжении периода времени, достаточного для отчетливого выявления, и эпизоды делирия. Вместе с этим у больного может наблюдаться снижение эмоционального контроля или мотивации, а также изменение социального поведения, проявляющееся минимум одним из четырех признаков:
- эмоциональная лабильность;
- раздражительность;
- апатия;
- огрубление социального поведения.
Для деменции умеренной степени выраженности характерны следующие изменения:
- Память: выраженная забывчивость, текущие события не остаются в памяти, а сохраняются лишь воспоминания о наиболее значимых событиях жизни.
- Ориентировка: пациент дезориентирован во времени и не полностью ориентирован на месте.
- Мышление: наблюдаются выраженные трудности при решении задач, в том числе анализе сходств и различий, что оказывает негативное влияние на повседневную активность.
- Взаимодействие с окружающими: у пациента утрачивается самостоятельность вне дома, он может вступать в общение под контролем других лиц.
- Поведение дома и увлечения: крайнее ограничение интереса, способность к выполнению только наиболее простых видов деятельности.
- Самообслуживание: снижение как инструментальной (возможность пользоваться бытовыми приборами), так и базисной (гигиена, одевание, приготовление пищи, передвижение) повседневной деятельности, трудности в самостоятельном проживании (однако пациента можно оставить на какое-то время одного); пациент нуждается в помощи при одевании, гигиенических процедурах и естественных отправлениях.
В случае, если выполняются общие критерии деменции, и при этом отсутствуют данные физического или специального обследования или данные из анамнеза о другой возможной причине деменции, системном заболевании или о злоупотреблении психоактивными веществами, то выставляется диагноз F00 – Деменция при болезни Альцгеймера.
В зависимости от возраста начала, степени прогредиентности, типа клинической симптоматики, особенно относительной выраженности симптомов поражения височной, теменной или лобной долей, типов нейропатологических или нейрохимических аномалий устанавливается подтип деменции при болезни Альцгеймера:
F00.0 – Деменция при болезни Альцгеймера с ранним началом.
F00.1 – Деменция при болезни Альцгеймера с поздним началом.
F00.2 – Деменция при болезни Альцгеймера, атипичная или смешанного типа.
Если выполняются общие критерии деменции, но при этом отмечается неравномерность поражения высших корковых функций, а также имеется минимум один из признаков очагового поражения мозга, либо имеются данные анамнеза, обследования и тестирования о наличии цереброваскулярного заболевания, которое обоснованно могло бы засчитаться этиологически связанным с деменцией, то рассматривается возможность установления диагноза сосудистой деменции F01:
F01.0 – Сосудистая деменция с острым началом.
F01.1 – Мульти-инфарктная деменция.
F01.2 – Подкорковая сосудистая деменция.
F01.3 – Смешанная корковая и подкорковая сосудистая деменция.
Дифференциальная диагностика сосудистой деменции и болезни Альцгеймера основана на выявлении различий в факторах риска, особенностей начала и течения патологии, а также наличии и выраженности сопутствующих когнитивных, аффективных, двигательных и тазовых нарушений (Таблица 2).
Таблица 2. Дифференциальная диагностика сосудистой деменции и болезни Альцгеймера
| Признаки | Сосудистая деменция | Болезнь Альцгеймера |
| Сосудистые факторы риска | Всегда присутствуют | Могут присутствовать |
| Начало | Острое, подострое, постепенное | Постепенное |
| Течение | Ступенеобразное, с периодами стабилизации и регресса симптомов | Прогрессирующее, иногда с периодами кажущейся стабилизации |
| Когнитивные нарушения | Преобладают симптомы дисфункции подкорковых и лобных отделов (брадифрения, нарушения регуляции, планирования, изменение поведения, двигательные нарушения) | Преобладают симптомы дисфункции височно-теменной области (амнезия, афазия, нарушение пространственных функций) |
| Аффективные нарушения | Отмечаются часто, развиваются рано | Отмечаются реже, развиваются позднее |
| Двигательные нарушения | Часто развиваются на ранней стадии | Возможны на поздней стадии |
| Тазовые нарушения | Часто появляются на ранней стадии | Появляются на поздней стадии |
При сосудистой деменции практически всегда наблюдаются двигательные расстройства, в первую очередь нарушениями походки, которая становится шаркающей и семенящей, а при нарастании деменции нарушается инициация ходьбы – пациент не может сделать первый шаг, топчется на месте: ноги не отрываются от пола, а скользят по нему («походка лыжника»), грубо страдает поддержание равновесия. И хотя при этом типе деменции крайне редко наблюдается нарушение ориентировки в пространстве, при исследовании пространственного гнозиса и праксиса могут выявляться достаточно выраженные нарушения, связанные с трудностью планирования и организации деятельности.
Аналогично, дифференциальный диагноз деменции с тельцами Леви и болезни Альцгеймера основывается на выявлении различий в возрасте начала деменции (деменция с тельцами Леви начинается позднее, чем болезнь Альцгеймера), ранних симптомов (деменция с тельцами Леви часто манифестирует с двигательных нарушений, а болезнь Альцгеймера – с расстройств памяти), особенностях когнитивных нарушений и чувствительности к антипсихотикам (Таблица 3).
Таблица 3. Дифференциальный диагноз деменции с тельцами Леви и болезни Альцгеймера
| Признаки | Деменция с тельцами Леви | Болезнь Альцгеймера |
| Возраст начала деменции | Более позднее начало, чем при болезни Альцгеймера, старше 70 лет | Пик начала заболевания – 60-70 лет |
| Течение заболевания | Характерны флуктуации когнитивных нарушений | Постепенное ухудшение когнитивного функционирования |
| Ранние симптомы | Часто начинается с двигательных нарушений | Начало с расстройств памяти |
| Двигательные нарушения | Характерны первичные двигательные экстрапирамидные симптомы | Экстрапирамидные нарушения возникают существенно позже когнитивных расстройств |
| Особенности когнитивных нарушений | Выраженные оптико-пространственные расстройства, при относительно сохранной слухоречевой памяти | Нарушения памяти и других высших корковых функций |
| Галлюцинации | Зрительные галлюцинации на ранних этапах болезни | Галлюцинации встречаются редко и характерны для поздних стадий деменции |
| Чувствительность к антипсихотикам | Крайне чувствительны. Минимальные дозы нейролептиков приводят к резкому ухудшению состояния по типу акинетического криза | Применяют с осторожностью при соответствующих показаниях |
Наконец, дифференциальный диагноз лобно-височной деменции и болезни Альцгеймера основывается на оценке выраженности нарушений памяти и речи, изменений личности, моторных навыков, поведения и осознания болезни (Таблица 4).
Таблица 4. Дифференциальный диагноз лобно-височной деменции и болезни Альцгеймера
| Признаки | Лобно-височная деменция | Болезнь Альцгеймера |
| Память | Сохраняются почти в полном объеме довольно долго. | Нарушается на ранних этапах болезни. |
| Изменения личности | Глубокие изменений личности на ранних этапах болезни | Малозаметны на ранних этапах, затем становятся очевидны. |
| Речь | Рано утрачиваются речевые функции | Нарушаются на поздних стадиях |
| Моторные навыки (праксис) | Долго остаются способность выполнять привычные действия и простейшие профессиональные навыки | Возможны нарушения праксиса на ранних стадиях заболевания. |
| Поведение | Расторможенное поведение, нарушение основных социальных норм. | Нарушается на поздних стадиях |
| Сознание болезни | Полное отсутствие критики | Присутствие критики (чаще формальное) на ранних стадиях, утрата критики на поздних стадиях |
Например, на стадии мягкой деменции при лобно-височной деменции гораздо более выражены нарушения аппетита, апатия, аберрантное моторное поведение и расторможенность (также может наблюдаться эйфория), в то время как при болезни Альцгеймера более выражены тревога, симптомы депрессии, агрессия, нарушения сна, галлюцинации и бредовые расстройства.
После установления диагноза рекомендовано применение психообразовательных методов для информирования родственников больного о характере заболевания, его течении, прогнозе и методах лечения. В частности, пациенту и родственникам необходимо разъяснить необходимость и режим приема базисных средств для лечения деменции, рассказать об ожидаемом терапевтическом эффекте. Прием лекарственных средств должен осуществляться под контролем ухаживающего лица, поскольку сам больной может быть недостаточно критичен, чтобы самостоятельно выполнять рекомендации.
Из-за тяжести заболевания и снижения интеллекта пациенту также требуется модификация окружающей среды, в которой он живет. Например, может возникнуть необходимость в переоснащении квартиры (например, улучшенное освещение, таблички на дверях туалета и ванной, камеры наблюдения, краны с термостатом, датчики контроля уровня воды в раковинах и ванной, отказ от газовой плиты при ее наличии или ее замена на модифицированную и безопасную модель). Из-за сложностей в уходе за пациентом следует рассмотреть возможность найма сиделки или размещение в специализированном заведении (дом престарелых, интернат), где пациенту могут обеспечить полноценный уход.
Независимо от типа деменции, фармакотерапия направлена, в первую очередь, на снижение прогрессирования когнитивных нарушений и общего функционирования больного. Согласно Федеральным клиническим рекомендациям по диагностике и лечению болезни Альцгеймера, основные стратегии патогенетической терапии болезни Альцгеймера включают холинергическую, глутаматергическую и нейротрофическую. При этом как указано в Федеральных клинических рекомендациях «Когнитивные расстройства у лиц пожилого старческого возраста» основой терапии болезни Альцгеймера является применение базисных препаратов – антихолинэстеразных средств и мемантина.
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило 5 отдельных лекарств и одну комбинацию лекарств для лечения болезни Альцгеймера: среди ингибиторов ацетилхолинэстеразы – это донепезил, галантамин и ривастигмин для лечения легкой и умеренной болезни Альцгеймера; в группе антагонистов NMDA рецепторов – мемантин для умеренной и тяжелой болезни Альцгеймера; Адуканумаб (Адухельм) – моноклональное антитело, нацеленное на Aβ (первый препарат, одобренный FDA почти за два десятилетия). Донепезил и мемантин одобрены для комбинированного применения. Ингибиторы ацетилхолинэстеразы входят в первую линию терапии болезни Альцгеймера. Вторую линию терапии составляет мемантин или его комбинация с ингибиторами ацетилхолинэстеразы, церебролизином или ривастигмином (Рис. 4).
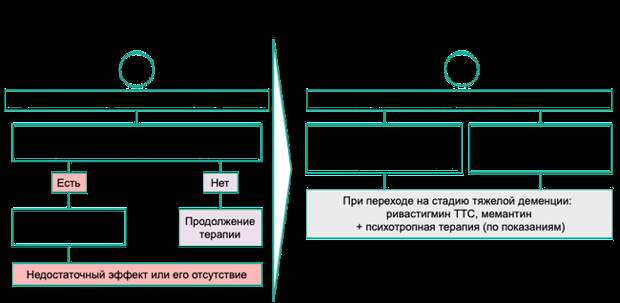
Рисунок 4. Алгоритм терапии болезни Альцгеймера. АХЭ – ацетилхолинэстераза.
Из группы ингибиторов ацетилхолинэстеразы (1++, А) второго поколения – донепезил, ривастигмин и галантамин (УУР – А, УДД – 1) – применяются для преодоления холинергической недостаточности при болезни Альцгеймера. Назначение комбинированной терапии антихолинэстеразными средствами, например, донепезилом и блокаторами глутаматных NMDA-рецепторов, рекомендуется пациентам с умеренно тяжелой деменцией при болезни Альцгеймера (5-14 баллов по шкале MMSE).
Донепезил принимается один раз в сутки по 5 мг (1 таблетка, 5 мг) вечером перед сном, независимо от приема пищи, в течение 4-6 недель. Контроль эффекта и переносимости терапии проводится через один месяц. В случае хорошей переносимости и наличия положительного клинического эффекта дозу увеличивают до 10 мг в сутки (1 таблетка, 10 мг). Критерием эффективности ацетилхолинергической терапии считают улучшение или стабилизацию симптомов на протяжении 6 и более месяцев. Если при использовании одного антихолинэстеразного средства положительный эффект отсутствует, его следует заменить другим препаратом этой же группы. У пациентов с болезнью Альцгеймера рекомендуется как можно более длительная терапия антихолинэстеразными средствами.
Донепезил показал хороший эффект в отношении коррекции когнитивной дисфункции. В частности, донепезил (Алзепил) нормализовал когнитивные функции (увеличение суммы баллов по шкале MMSE и снижение – по Когнитивной шкале оценки болезни Альцгеймера ADAS-cog) и повседневное функционирование (увеличение баллов по шкале Disability Assessment for Dementia, DAD) пациентов на 4-12 недели терапии, а также улучшал показатели общего клинического впечатления по шкале CGI-C (Clinical global impression). Для получения оптимального эффекта антихолинэстеразной терапии следует применять препараты в максимально переносимых дозах (УУР – А, УДД – 1) и на протяжении как можно более длительного периода (УУР – В, УДД – 2). При выборе ингибитора ацетилхолинэстеразы следует учитывать профиль побочных эффектов и характер лекарственных взаимодействий (УУР – А, УДД – 1).
Основные принципы терапии ингибиторами ацетилхолинэстеразы включают:
- Дозозависимость клинических эффектов ингибиторов ацетилхолинэстеразы в пределах терапевтического диапазона, поэтому целесообразно назначение максимальной рекомендуемой поддерживающей дозы препарата.
- Этапность терапии от стартовой до поддерживающей дозы с периодом титрования 4-6 недель.
- Пробная терапия – первые 3-6 месяцев. Далее проводится первоначальная оценка эффективности.
- Контроль эффективности долгосрочной терапии должен проводиться каждые 6 месяцев.
- Терапия является длительной (т.е. многолетний прием при условии его удовлетворительной эффективности и переносимости).
Среди блокаторов глутаматных NMDA-рецепторов препаратом первой линии при умеренной и тяжелой деменции, а также и на стадии легкой деменции в качестве монотерапии или в комбинации с ингибиторами ацетилхолинэстеразы, является мемантин. Препарат принимается один раз в сутки по 5 мг утром в одно и то же время, независимо от времени приема пищи. Через неделю доза увеличивается до 10 мг, в течение третьей недели – до 15 мг, на четвертой неделе – до 20 мг (максимальная суточная и разовая доза). Поддерживающую терапию можно продолжать до тех пор, пока сохраняется терапевтический эффект, который необходимо регулярно оценивать. Для улучшения комплаенса следует делать акцент на том, что базисная терапия требует постоянного приема, поскольку эффект от терапии не мгновенный и может быть малозаметен.
Все пациенты с расстройствами памяти и другими когнитивными нарушениями любой выраженности должны проходить диагностическое обследование, поскольку снижение когнитивных функций не может считаться нормальным в любом возрасте, а лечение должно начинаться немедленно после постановки диагноза и проводиться длительно на оптимальных терапевтических дозах с соблюдением предписанного режима лечения. При назначении терапии необходимо следовать рекомендованным стандартам. В рамках стандартов также важны индивидуализации терапии и мониторинг терапевтического эффекта. Эффективность терапии на стадии умеренной деменции может быть повышена за счет комбинированной терапии (ингибиторы ацетилхолинэстеразы + мемантин). Для повышения комплаентности необходимо просвещать семью больного о критериях эффективности лечения болезни Альцгеймера и целях обеспечения долговременности терапии.
Важно понимать, что терапия не способна полностью излечить и восстановить утраченные функции, а направлена на замедление прогрессирования заболевания и предотвращение полной утраты функций. На этом этапе для защиты больного и его семьи может потребоваться официальное оформление его недееспособности и опекунства над ним. Чем раньше будет выявлена деменция, тем больше вероятность того, что терапия окажет положительный эффект. Это еще раз подчеркивает особую актуальность проблемы ранней диагностики и терапии когнитивных нарушений у пожилых пациентов.
Пять финальных максим нейропсихиатрического континуума
Итоги симпозиума подвел Олег Семенович Левин, представив 5 главных проблем нейропсихиатрического континуума. Эксперт отметил, что современная медицина невозможна без количественной, многомерной, «объективной» оценки с помощью шкал, которые представляют собой компромисс между качественной клинической оценкой и ее количественным выражением (Максима 1).
Уходит искусство клинического описания, изобилующее деталями, нюансами, качественными закономерностями – торжествует «бухгалтерский» статистический подход, знаменующий победу общего и частого над частным.
Шкалы позволяют не только выявить, но и оценить гетерогенность аффективных нарушений, в том числе депрессии (Максима 2), как врачами-психиатрами и неврологами, так и специалистами первичного звена. При этом шкалы в большей степени нацелены на исключение, а не подтверждение какого-либо заболевания. К тому же результат оценки будет определяться и типом шкалы, что может вызвать трудности в «тонкой» дифференциации различных подтипов первичной и вторичной депрессии.
Первичная (идиопатическая) депрессия включает:
- униполярную (рекуррентную) депрессию
- большую/малую депрессию
- биполярное расстройство
- дистимию
- «маскированную» депрессию
Вторичная депрессия подразделяется на:
- реактивную (невротическую) депрессию (псевдодепрессивная симптоматика в рамках соматоформного расстройства)
- преморбидное расстройство личности («меланхолический тип личности», «статотимия»)
- псевдодепрессию (апатия, аффективная диспросодия, насильственный плач, деменция)
Несмотря на частые когнитивные жалобы, при объективном нейропсихологическом исследовании у большинства больных с депрессией либо не отмечается существенных отклонений, либо отмечается флуктуирующее нарушение выполнения тестов, требующих усилия и мотивации. Лишь у части пациентов с депрессией вызываются стойкие когнитивные нарушения, преимущественно лобного типа, которые указывают на параллельно развивающееся сопутствующее когнитивное расстройство, которое может быть обусловлено тем же органическим поражением мозга («депрессия-плюс»). Интересно, что в клинической практике ошибочная диагностика депрессии у пациента с развивающейся деменцией наблюдается чаще, чем ошибочная диагностика деменции у пациента с депрессией (Максима 3).
Пациентам с депрессией и когнитивными нарушениями угрожает развитие деменции в будущем. Когнитивный дефицит (забывчивость, нарушение внимания и планирования, низкая мотивация, замедленность реагирования, снижение приверженности терапии и резистентность к лечению, увеличение частоты рецидивов) при этом может служить независимым предиктором исхода депрессии. С другой стороны, при первичных аффективных нарушениях вероятность развития когнитивных расстройств не увеличивается или увеличивается незначительно (Максима 4).
В этой связи особую сложность представляет выбор теста для оценки когнитивных функций у больных с деменцией и депрессией, поскольку когнитивные нарушения и аффективные расстройства редко протекают независимо и обусловлены общими механизмами, а структура депрессивной симптоматики меняется при прогрессировании деменции (Рис. 5).
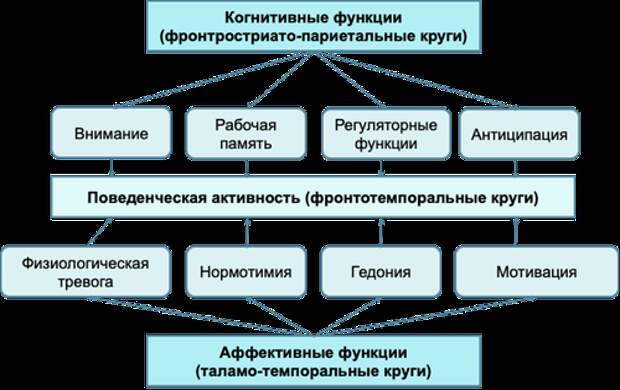
Рисунок 5. «Пересечение» когнитивных, аффективных и поведенческих нарушений.
Низкая эффективность когнитивного теста может быть связана с наличием функциональных когнитивных расстройств или депрессивной псевдодеменции. Выявить депрессивную псевдодеменцию можно по «красным флажкам»: острому или подострому развитию, быстрому прогрессированию симптомов, указаний на предшествующую психическую патологию, настойчивые жалобы пациента на снижение интеллектуальных способностей, отсутствие усилия при выполнении тестов («не знаю») и их вариабельность, а также нарушение выполнения тестов, требующих скорости реакции, концентрации и устойчивости внимания, планирования, мотивации и волевого усилия. Главным критерием данного состояния является нормализация когнитивных функций при применении антидепрессантов.
Эффективность терапии тревожных расстройств также во многом определяется спецификой центральных и нейромедиаторных механизмов систематизации тревоги (Рис. 6).
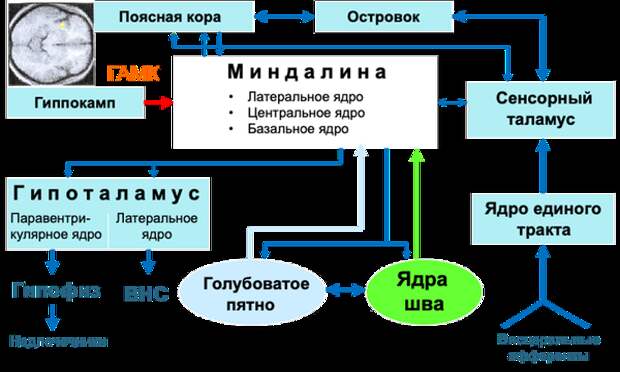
Рисунок 6. Центральные механизмы систематизации тревоги.
Таким образом, основная трудность при оценке состояния больного и дифференциальной диагностике психоневрологических нарушений заключается в сложности, неоднородности и взаимозависимости трех основных компонентов нейропсихиатрического континуума – аффективных состояний, включающих тревогу, депрессию и апатию, когнитивных (легкие нарушения, переходный когнитивный синдром, деменция) и поведенческих нарушений (расторможенность, агрессивность, абулия). В этой связи врачу важно помнить, что независимо от природы обнаруженных нарушений, наиболее эффективной терапии способствует максимально полная компенсация всех имеющихся нейротрансмиттерных механизмов (Максима 5; Рис. 7). Поэтому приоритетным становится использование препаратов, способных воздействовать сразу на несколько нейротрансмиттерных систем, например, венлафаксин (Велаксин), который в дозах от 75 до 125 мг/сут проявляет преимущественно серотонинергическое действие, при повышении дозы до 225 мг/сут включается норадренергическое действие, а дальнейшее повышение дозы до 375 мг приводит к появлению дофаминергического эффекта.
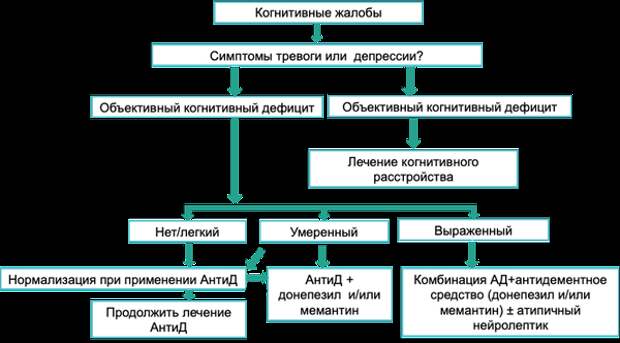
Рисунок 7. Алгоритм выбора средств фармакотерапии депрессии и когнитивных нарушений. АнтиД – антидепрессанты.
Свежие комментарии