
Железодефицит (ДЖ) является одной из наиболее актуальных на сегодняшний день проблем здравоохранения в связи со своей высокой распространенностью и частотой негативных последствий для здоровья человека [1]. Так, железодефицит служит не только основным этиологическим фактором анемии, но и лежит в основе большого количества разнообразных симптомов, которые нередко становятся причиной диагностических ошибок и рассматриваются как проявления других заболеваний [1].
Железодефицитная анемия (ЖДА) считается самостоятельной нозологической формой, а латентный дефицит железа (ЛДЖ) относится к функциональным нарушениям обмена железа, предшествующим ее развитию [1]. По данным экспертов Всемирной организации здравоохранения, дефицит железа занимает первое место среди 38 наиболее распространенных заболеваний человека, и от ДЖ страдает примерно каждый третий житель планеты [2]. ЖДА составляют 80% от всех анемий у взрослых [3, 4].
В последнее время все активнее исследуется вопрос о взаимосвязи дефицита железа и наличия инфекции Helicobacter pylori (HP) [1, 5-8]. Зависимость между инфекцией H. pylori (НР) и ЖДА была продемонстрирована рядом крупных эпидемиологических исследований, которые, в частности, выявили, что при наличии HP риск развития анемии увеличивается в 1,19, а риск анемии средней и тяжелой степени – в 1,39 раз [7]. Таким образом, сегодня уже не вызывает сомнений, что анемия является осложнением НР инфекции, и эрадикация возбудителя приводит к улучшению течения ЖДА и большей восприимчивости к терапии препаратами железа [1, 5, 6]. Результаты многочисленных исследовании позволили экспертам включить в Маастрихтский V/Флорентийский консенсус, соответствующее положение: «Существует доказательство связи Н. pylori и необъяснимой железодефицитной анемии, тромбоцитопенической пурпуры и дефицита витамина В12. При этих заболеваниях следует искать Н. pylori и проводить его эрадикацию» [8].
Современный взгляд на причины железодефицита
Железо – незаменимый биометалл для человека, играющий ключевую роль в функционировании клеток многих систем организма. Железо принимает участие в окислительно-восстановительных процессах, реакциях свободнорадикального окисления, росте и старении тканей, механизмах общей и тканевой резистентности, кроветворении, снабжении органов и тканей кислородом, активации и ингибировании ряда ферментов [9]. Дефицит железа закономерно отражается на умственной, физической, неврологической, терморегулятивной функциях; нарушаются поведение и способность к обучению; снижаются толерантность к физическим нагрузкам и познавательные способности [10, 11].
Железодефицит – состояние полиэтиологическое, связанное с нарушением поступления железа, его усвоения или повышенных потерь [3]. У женщин, например, основными причинами развития ЖДА служат обильные менструальные кровотечения, беременность, роды и лактация. Для женщин в постменопаузе и у мужчин ведущей причиной железодефицита является кровопотеря из желудочно-кишечного тракта. Дефицит железа может развиться и без кровопотери, например, при растительной диете, вследствие резекции желудка или кишечника, или в результате нарушения всасывания железа у лиц с воспалительными заболеваниями кишечника [3, 4].
Железодефицит является не только основным этиологическим фактором анемии, но и приводит у пациента к развитию большого количества разнообразных симптомов [12]:
- слабость, повышенная утомляемость, невнимательность, беспокойство, забывчивость, раздражительность;
- утренние головные боли, обмороки, головокружения;
- повышенная восприимчивость к инфекциям;
- бледность и сухость кожи, слизистых оболочек;
- трещины в углах рта, стоматит;
- ломкость ногтей и волос;
- одышка (как при физических нагрузках, так и в покое);
- нарушение пищеварения, плохой аппетит, метеоризм, нарушения стула, трудности глотания;
- извращение вкуса и обоняния.
Наряду с недостаточностью железа в продуктах питания, нарушением всасывания железа и хронической кровопотерей, важная роль в развитии ДЖ отводится нарушениям метаболизма железа при хроническом воспалении [1]. Большое значение в патогенезе такого «функционального» ДЖ имеет гепсидин [13]. Гепсидин — 25-аминокислотный пептид, синтезируемый в печени и определяемый в плазме крови и моче, участвует и в метаболизме железа, и в антибактериальной защите. Увеличение синтеза гепсидина в печени под влиянием провоспалительных цитокинов при хронических заболеваниях приводит к снижению абсорбции железа в кишечнике и блокированию его высвобождения из макрофагов (вследствие блокады гепсидином функции ферропортина) [14, 15]. В таком случае развивается не истинный или абсолютный дефицит железа, а функциональный или перераспределительный, характеризующийся сочетанием пониженного содержания железа в плазме крови и повышенного его уровня в клетках ретикулоэндотелиальной системы [1, 5].
Роль Helicobacter pylori в развитии железодефицита
Хеликобактерная инфекция сегодня отличается очень высокой распространенностью: согласно данным последних лет она диагностируется у 65-92% взрослых [16]. Частота формирования хронического хеликобактерного гастрита обусловливает и частоту развития других заболеваний, ассоциированных с H. pylori, как желудочных (например, рак желудка), так и внежелудочных (кардиоваскулярной и неврологической патологии, кожных болезней, рака легкого, MALT-лимфомы, идиопатической тромбоцитопенической пурпуры и железодефицитной анемии) [16, 17]. Обзор (NHANES) показал, что с инфекцией H. pylori могут быть связаны 32,3% случаев железодефицитной анемии и 13,6% железодефицита [18]. Крупномасштабные исследования, включившие более 1800 и более 7000 пациентов, показали, что в группе пациентов с инфекцией НР отмечалось снижение уровня ферритина в 17% и в 13,9% случаев, соответственно [19, 20]. Еще одно исследование, включившее около 3000 человек, продемонстрировало, что у мужчин и женщин с инфекцией H. pylori после менопаузы, отмечались более низкие средние уровни ферритина сыворотки, чем у больных, неинфицированных НР [21].
Современная концепция патогенеза анемии у больных с НР инфекцией включает сочетание 5 возможных механизмов [12]:
- хроническая кровопотеря на фоне эрозивно-язвенных изменений слизистой желудка и двенадцатиперстной кишки [22]. Скрытые потери крови возможны и без развития желудочно-кишечного кровотечения, за счет микропотерь при эрозивном и геморрагическом гастрите [23].
- бактериальная секвестрация свободного железа, ингибирование свободного всасывания поступающего в организм железа [24, 25].
- микробное обсеменение желудка НР требует большого количества железа для роста бактерий и приводит к использованию железа хозяина [26].
- атрофия слизистой желудка на фоне инфекции приводит к нарушению высвобождения и всасывания железа из продуктов питания. Кислотность желудочного сока выше 5,5 обеспечивает адекватное всасывание железа, а снижение кислотности, соответственно, способствует развитию ДЖ. Кроме того, НР инфекция приводит к снижению уровня витамина С, что также влияет на всасывание железа в кишечнике [27-29].
- развитие анемии хронического воспаления за счет синтеза провоспалительных цитокинов [1, 12]. Развитие анемии хронического воспаления тесно связано с повышением уровня гепсидина, который сегодня считается маркером острой фазы воспаления в слизистой оболочке желудка [1, 30]. Было также показано, что концентрация предшественника гепсидина – прогепсидина, повышается при H. pylori инфекции и снижается после ее эрадикации [31].
Закономерно, что железодефицитная анемия неуточненного генеза, согласно российским и международным клиническим руководствам по хеликобактерной инфекции, требует проведения диагностического поиска для выявления H. pylori и его эрадикации [16, 32, 33]. По имеющимся данным, результаты такого подхода улучшают гематологические показатели и способствуют повышению эффективности последующей ферротерапии [34-36].
Особенности диагностики латентного дефицита железа
Развитию ЖДА предшествует период латентного железодефицита, характеризующегося низкими показателями сывороточного железа и ферритина на фоне нормального уровня гемоглобина [1].
Диагностика ЛДЖ представляет определенные трудности при наличии фактора воспаления [1]. Уровень ферритина действительно прямо пропорционален количеству железа в макрофагах и гепатоцитах, но только при отсутствии инфекции или воспалительного процесса. При воспалении у пациентов уровень ферритина может быть нормальным или даже повышенным в связи с повышением запасов железа в ретикуло-эндотелиальной системе, а также в связи с тем, что ферритин является провоспалительным цитокином, и его экспрессия индуцируется воспалением. [37].
Уровень сывороточного железа также не позволяет точно дифференцировать ЖДА и анемию хронического воспаления. Истинный дефицит железа наблюдается у пациентов, страдающих заболеваниями, приводящими к хронической кровопотере (онкологическими, воспалительными заболеваниями ЖКТ и т.д), и при назначении препаратов железа таким пациентам наблюдается быстрое его потребление эритроидными клетками-предшественниками, активация эритропоэза и компенсация анемии. В то же время при функциональном дефиците железа такое лечение не даст видимого результата [1].
Поскольку уровень ферритина не является стабильным показателем запасов железа у пациентов с воспалительными процессами, в рекомендациях ВОЗ критическими значениями уровня для ферритина при диагностике ЛДЖ определены 15 мкг/мл у здоровых людей и 70 мкг/мл при наличии инфекционных и воспалительных заболеваний [1, 38].
Исследование взаимосвязи между инфекцией H. pylori и латентным дефицитом железа
В наши дни активно продолжаются исследования, устанавливающие связь между ЛДЖ и H. pylori и изучающие основные этиопатогенетические варианты развития дефицита железа у больных с данной инфекцией.
В работе Е.В. Ших и соавт. [1] была проанализирована частота латентного железодефицита у 606 больных с инфекцией НР. Латентный дефицит железа, который диагностировался при снижении насыщения трансферрина железом (НТЖ) менее 17%, и/или снижении уровня ферритина менее 70 мкг/л, при отсутствии анемии, был обнаружен у 66 (10,9%) пациентов [1].
При том, что сывороточное железо и НТЖ у всех 66 больных соответствовали критериям ЛДЖ, другие показатели продемонстрировали интересное расхождение. Так, средний объем эритроцитов (MCV) и содержание гемоглобина в эритроците (MCH) у 62,1% больных оставался в пределах нормы, а у 37,9% пациентов снижались, что свидетельствовало о развивающемся дефиците железа в эритроцитах. Уровень ферритина у 66,7% не превышал 70 мкг/л, у 19,7% пациентов он был ниже 15 мкг/л, и у 33,3% был выше 70 мкг/л и достигал 254,2 мкг/л. Такой же значительный разброс среди больных с ЛЖД наблюдался и по уровню гепсидина крови: у 45,5% больных значения гепсидина в крови не превышали 26 нг/мл, а у 54,5% он был повышен, максимально до 91,1 нг/мл [1].

Такие результаты позволили исследователям распределить больных с ЛЖД на три подгруппы, соответствующие различным патогенетическим механизмам развития железодефицита [1]:
- Пациенты с истинным дефицитом железа (19,7%): при уровне ферритина ниже 15 мкг/л и нормальном значении гепсидина в крови.
- Пациенты с «комбинированным» железодефицитом (47%): при уровне ферритина от 30 до 70 мкг/л. В данном случае истинный железодефицит сочетался с отчетливым воздействием воспаления (прежде всего, гепсидина).
- Пациенты, у которых развитие дефицита железа было обусловлено связанным с воспалением блокирующим влиянием гепсидина (33,3%): с уровнем гепсидина выше нормы и уровнем ферритина более 70 мкг/л.
Менеджмент пациентов с железодефицитом и H. pylori
Хронический хеликобактерный гастрит служит фоном для развития многочисленных заболеваний, ассоциированных с Н. pylori [16]. Поэтому, согласно действующим клиническим рекомендациям, эрадикационная терапия инфекции H. pylori показана при язвенной болезни желудка и двенадцатиперстной кишки, MALT-лимфоме желудка, пациентам перед или после эндоскопической резекции желудка, при гастропатиях, индуцированных приемом НПВС, при функциональной диспепсии, аутоиммунной тромбоцитопении и железодефицитной анемии [16].
Терапией первой линии для эрадикации H. pylori служит стандартная тройная терапия, включающая ингибитор протонной помпы (ИПП), кларитромицин и амоксициллин. В качестве альтернативы может быть выбрана классическая четырехкомпонентная терапия на основе висмута трикалия дицитрата в сочетании с ИПП, тетрациклином и метронидазолом. Еще один альтернативный вариант эрадикационной терапии первой линии: квадротерапия без препарата висмута, которая включает ИПП, амоксициллин, кларитромицин и метронидазол [16].
При наличии железодефицитного состояния целесообразно назначение и препаратов железа, например, Сорбифер Дурулес [1]. Сорбифер Дурулес (фармацевтическая компания «ЭГИС», Венгрия) – комбинированный препарат, обеспечивающий стимуляцию синтеза гемоглобина и повышающий продукцию эритроцитов костным мозгом. Сорбифер Дурулес содержит 320 мг железа сульфата безводного (что эквивалентно 100 мг двухвалентного железа) и 60 мг аскорбиновой кислоты [9, 39]. Входящий в состав препарата сульфат железа обладает высоким коэффициентом всасывания в ЖКТ и практически не образует малодоступных сложных соединений. Наличие аскорбиновой кислоты значительно улучшает всасывание и усвоение железа. Сульфат железа и аскорбиновая кислота в препарате Сорбифер Дурулес окружены трехразмерным пластиковым матриксом, имеющим поры. Этот матрикс под воздействием влажности постепенно становится проницаемым для соединения железа, и в течение 6 часов постепенно его высвобождает. После полного высвобождения опустевший носитель разрушается и элиминируется из кишечника. Пролонгированное высвобождение ионов двухвалентного железа из таблеток препятствует нежелательному повышению уровня ионов железа в ЖКТ и их раздражающему действию на слизистую оболочку [9, 39].

Клинические доказательства эффективности Сорбифер Дурулес
Возможности применения Сорбифер Дурулес при ДЖ на фоне HP инфекции были изучены в той же работе Е.В. Ших и соавт. [1]. Пациентам проводили эрадикацию НР в течение 14 дней с помощью схемы квадротерапии с висмутом. Для лечения железодефицита использовали Сорбифер Дурулес – по 1 таблетке в день в течение 1 месяца.
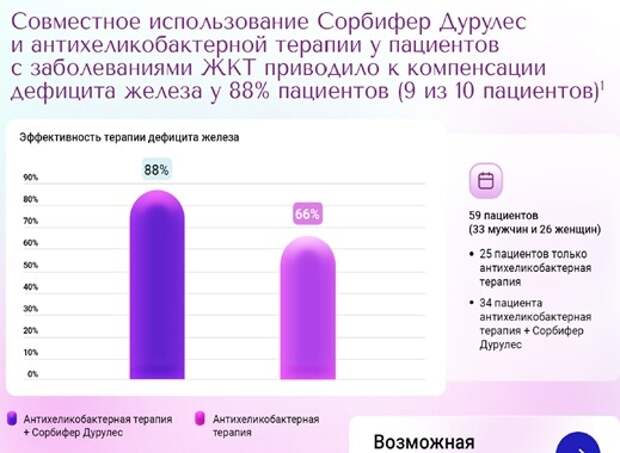
При проведении антихеликобактерной терапии + Сорбифер Дурулес дефицит железа был купирован у 88% больных [1]. В то же время, у пациентов, получавших только антихеликобактерную терапию, дефицит железа отсутствовал в 60% случаев, а при терапии только Сорбифер Дурулес терапия была эффективна у 57% [1].
Эрадикации НР была эффективна у 71% пациентов, а у 29% при повторном исследовании на НР тесты были положительными. Интересно, что у большинства пациентов с неэффективной эрадикацией HP отмечалась и низкая эффективность терапии дефицита железа [1]. Более детальный анализ показал, что отсутствие успеха в эрадикации HP уменьшало успех терапии железодефицита у пациентов с ДЖ хронического воспаления и ДЖ «комбинированного» типа. У больных с истинным дефицитом железа терапия препаратами железа была эффективна в 100% случаев. Таким образом, наиболее вероятной причиной сохранения дефицита железа было неэффективное лечение воспаления, обусловленного НР, и сохранение отрицательного влияния гепсидина на метаболизм железа [1].
Заключение
Инфекция Helicobacter pylori является одним из факторов риска развития латентного железодефицита. Наличие инфекции HP значительно увеличивает риск снижения цветовых показателей крови, критического уменьшения уровня ферритина, и развития железодефицитной анемии. В наши дни ЖДА является показанием для назначения эрадикационной терапии. Эрадикация Helicobacter pylori с помощью классических схем помогает нормализовать показатели железа крови у 60% больных. Назначение препаратов железа помогает повысить эффективность терапии: так, Сорбифер Дурулес в сочетании с эрадикационной терапией позволяет купировать железодефицит у 88% пациентов.
Литература
- Патогенетические варианты латентного дефицита железа и эффективность терапии у больных с инфекцией Н.Pylori [Текст] / Е. В. Ших, В. Н. Дроздов, Н. В. Шулятьева // Поликлиника: Профессиональный журнал для руководителей и врачей всех специальностей ЛПУ России. — 2021. — № 2. — С. 10-14.f
- Kassebaum NJ, Jasrasaria R, Naghavi M, et al. 2014. A systematic analysis of global anemia burden from 1990 to 2010. Blood 123: 615–624.
- Клинические рекомендации – Железодефицитная анемия – 2021- 2022-2023 (09.09.2021) – Утверждены Минздравом РФ
- Идельсон ЛИ, Воробьев ПА. Железодефицитные анемии. Руководство по гематологии. Под ред. В.И. Воробьева, Москва, Ньюдиамед; 2005, p. 171-90.
- А.А. Левина, Т.В. Казюкова, Н.В. Цветаева и др., Педиатрия, № 1, 67-74 (2008).
- Hu, Y. et al. Study on the anemia status of Chinese urban residents in 2010–2012. Chin J Prev Med 50, 213–216 (2016).
- Курилович С.А., Решетников О. В. Эпидемиологические исследования в гастроэнтерологии: многолетний сибирский опыт изучения Helicobacter pylori и ассоциированных заболеваний. Эксперим. И клин. гастроэнтерология. – 2015. – № 3. – С. 4–10.
- Старостин Б.Д. Лечение Helicobacter руlогі-инфекции – Маастрихсткий V/Флорентийский консенсусный отчет (перевод с комментариями) // Гастроэнтерология Санкт-Петербурга. 2017; (1): 2-22.
- Ломова Н.А., Дубровина Н.В., Кан Н.Е., Тютюнник В.Л. Быстрая коррекция дефицита железа у беременных: обзор современных возможностей // РМЖ. Мать и дитя. 2017. №2. URL: https://cyberleninka.ru/article/n/bystraya-korrektsiya-defitsita-zheleza-u-beremennyh-obzor-sovremennyh-vozmozhnostey (дата обращения: 22.04.2024).
- Breymann C., Honegger C., Holzgreve W., Surbek D. Diagnosis and treatment of iron-deficiency anaemia during pregnancy and postpartum // Arch. Gynecol. Obstet. 2010. Vol. 282(5). P. 577–580.
- Choudhury N., Aimone A., Hyder S.M., Zlotkin S.H. Relative efficacy of micronutrient powders versus iron-folic acid tablets in controlling anemia in women in the second trimester of pregnancy // Food Nutr Bull. 2012. Vol. 33(2). P. 142–149.
- Шулятьева Н.В., Дроздов В.Н., Сереброва С.Ю., Стародубцев А.К., Ших Е.В. Значение инфекции h. pylori в развитии дефицита железа // ЭиКГ. 2018. №6 (154). URL: https://cyberleninka.ru/article/n/znachenie-infektsii-h-pylori-v-razvitii-defitsita-zheleza (дата обращения: 24.04.2024).
- C.H. Park, E.V. Valore, A.J. Waring, T. Ganz, Journal of Biological Chemistry, 276, 7806-7810 (2001); doi: 10.1074/jbc.M008922200.
- J. Arezes, E. Nemeth, International journal of laboratory hematology, 1, 92-98 (2015); doi: 10.1111/ijlh.12358.
- A.E. Armitage, L.A Eddowes, U. Gileadi, et al., Blood, 15, 4129-4139 (2011); doi: 10.1182/blood-2011-04-351957.
- Ивашкин В.Т., Маев И.В., Лапина Т.Л., Шептулин А.А., Трухманов А.С., Баранская Е.К., Абдулхаков Р.А., Алексеева О.П., Алексеенко С.А., Дехнич Н.Н.,. .. Цуканов В.В. Клинические рекомендации Российской гастроэнтерологической ассоциации по диагностике и лечению инфекции Helicobacter pylori у взрослых. Рос. ж. гастроэнтерол., гепатол., колопроктол. 2018;28(1):55-70. doi: 10.22416/1382-4376-2018-28-1-55-70
- Потапова Марина Валериановна, Скворцов Константин Юрьевич, Брояка Нелли Александровна, Конобеева Елена Владимировна РОЛЬ HELICOBACTERPYLORI В ПАТОГЕНЕЗЕ НЕКОТОРЫХ ГЕМАТОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ // Сибирский научный медицинский журнал. 2022. №3. URL: https://cyberleninka.ru/article/n/rol-helicobacterpylori-v-patogeneze-nekotoryh-gematologicheskih-zabolevaniy (дата обращения: 25.04.2024).
- Queiroz DMM, Harris PR, Sanderson IR, Windle HJ, Walker MM, Rocha AMC, Rocha GA, Carvalho SD, Bittencourt PF, de Castro LP, et al. Iron status and Helicobacter pylori infection in symptomatic children: an international multi-centered study. PLoS One 2013; 8: e68833; PMID:23861946; http://dx.doi.org/10.1371/ journal.pone.0068833
- Cardenas VM, Mulla ZD, Ortiz M, Graham DY. Iron deficiency and Helicobacter pylori infection in the United States. Am J Epidemiol 2006; 163:127-34; PMID:16306309; http://dx.doi.org/10.1093/aje/ kwj018
- Berg G, Bode G, Blettner M, Boeing H, Brenner H. Helicobacter pylori infection and serum ferritin: A population-based study among 1806 adults in Germany. Am J Gastroenterol. 2001 Apr; 96(4):1014-1018.
- Milman N, Rosenstock S, Andersen L, Jorgensen T, Bon-nevie O. Serum ferritin, hemoglobin, and Helicobacter pylori infection: a seroepidemiologic survey comprising 2794 Danish adults. Gastroenterology. 1998 Aug; 115(2):268-274.
- Yip, R. et al. Pervasive occult gastrointestinal bleeding in an Alaska native population with prevalent iron deficiency — Role of Helicobacter pylori gastritis. JAMA 277, 1135-1139 (1997).
- Blecker U, Renders F, Lanciers S, Vandenplas Y. Syncopes leading to the diagnosis of a Helicobacter pylori positive chronic active haemorrhagic gastritis. Eur J Pediatr 1991; 150:560-1; http://dx.doi.org/10.1007/BF02072207
- Rockey, D. C. & Cello, J. P. Evaluation of the Gastrointestinal-Tract in Patients with Iron-Deficiency Anemia. N Engl J Med 329, 1691-1695 (1993).
- Mubarak, N., Gasim, G. I., Khalafalla, K. E., Ali, N. I. & Adam, I. Helicobacter pylori, anemia, iron deficiency and thrombocytopenia among pregnant women at Khartoum, Sudan. Trans R Soc Trop Med Hyg 108, 380-384 (2014).
- Otto, B. R., Verweijvanvught, A. M. J. J. & Maclaren, D. M. Transferrins and Heme-Compounds as Iron Sources for Pathogenic Bacteria. Critical Reviews in Microbiology 18, 217-233 (1992).
- Muhsen K, BarakM, ShifnaidelL, Nir A, BassalR, Cohen D. Helicobacter pylori infection is associated with low serum ferritin levels in Israeli Arab children: a seroep-idemiologic study. J Pediatr Gastroenterol Nutr 2009; 49: 262-264.
- Annibale B, Capurso G, LahnerE, Passi S, RicciR, Maggio F, Delle Fave G. Concomitant alterations in intragastric pH and ascorbic acid concentration in patients with Helicobacter pylori gastritis and associated iron deficiency anaemia. Gut 2003; 52: 496-501.
- Choi JW. Serum-soluble transferrin receptor concentrations in Helicobacter pylori-associated iron-deficiency anemia. Ann Hematol 2006; 85: 735-737. Bini EJ. Helicobacter pylori and iron deficiency anemia: guilty as charged? Am J Med 2001; 111: 495-497.
- Azab SF, Esh AM. Serum hepcidin levels in Helicobacter pylori-infected children with iron-deficiency anemia: a case-control study. Ann Hematol 2013; 92(11): 1477-1483.
- Ozkasap S, Yarali N, Isik P, Bay A, Kara A, Tunc B. The role of prohepcidin in anemia due to Helicobacter pylori infection. Pediatr Hematol Oncol 2013; 30(5): 425-431.
- Malfertheiner P., Megraud F., O'Morain C.A., Gisbert J.P., Kuipers E.J., Axon A.T., Bazzoli F., Gas-barrini A., Atherton J., Graham D.Y.,. .. European Helicobacter and Microbiota Study Group and Consensus panel. Management of Helicobacter pylori infection — the Maastricht V/ Florence Consensus Report. Gut. 2017;66:6-30. doi: 10.1136/gutjnl-2016-312288
- Chey W.D., Leontiadis G.I., Howden C.W., Moss S.F. ACG Clinical Guideline: treatment of He-licobacter pylori infection. Am. J. Gastroenterol. 2017;112(2):212-239. doi: 10.1038/ajg.2016.563
- Tsay F.W., Hsu P.I. H. pylori infection and extra-gastroduodenal diseases. J. Biomed. Sci. 2018;25(1):65. doi: 10.1186/s12929-018-0469-6
- Tseng D.S., Li D., Cholleti S.M., Wei J.C., Jod-esty Y., Pham H.V. Effect of Helicobacter pylori treatment on unexplained iron deficiency anemia. Perm. J. 2019;23:18-195. doi: 10.7812/TPP/18-195
- Stasi R., Sarpatwari A., Segal J.B., Os-born J., Evangelista M.L., Cooper N., Provan D., Newland A., Amadori S., Bussel J.B. Effects of eradication of Helicobacter pylori infection in patients with immune thrombocytopenic purpura: a systematic review. Blood. 2009;113:1231-1240. doi: 10.1182/ blood-2008-07-167155
- Е.Н. Охотникова, Е.В. Поночевная, Клиническая иммунология. Аллергология. Инфектология, № 5/6, 22-24 (2012).
- WHO guideline on use of ferritin concentrations to assess iron status in individuals and populations. URL: https://www.who.int/publications/i/item/9789240000124 (дата обращения 24.04.2024)
- ИМП ЛП Сорбифер Дурулес. РУ ЛП-N (000080) – (РГ-RU) от 11.08.2022.
Свежие комментарии