Неблагоприятные факторы среды и старение приводят к нарушениям обучения, памяти и когнитивных функций, лежащих в основе адаптивного поведения. Нейрогенез — процесс появления нейронов из стволовых клеток мозга — тоже легко нарушается этими воздействиями. Однако до сих пор связь между способностью животных быстро изменять поведение, приспосабливаясь к меняющимся обстоятельствам, — когнитивной гибкостью — и нейрогенезом была изучена мало. В серии работ мы исследовали, как в условиях подавленного нейрогенеза меняется способность животных адаптироваться к новым условиям обучения. Для этого нами была разработана модель обучения в водном лабиринте Морриса, в которой животные должны были выучивать периодически меняющееся положение скрытой под водой платформы. Нам удалось выяснить, что в результате облучения и естественного старения у животных с пониженным нейрогенезом страдала когнитивная гибкость, однако первоначальное обучение не было нарушено, а дополнительное обучение позволяло животным со сниженным нейрогенезом «догнать» контрольные группы. Кроме того, мы обнаружили существование корреляций между уровнем нейрогенеза и поведенческими показателями: чем больше взрослорожденных нейронов сохранялось у пожилых животных, тем лучше были их показатели в задачах, требующих проявления когнитивной гибкости.
Представьте себе одну из ситуаций. На соседней улице развернулась стройка, из-за которой отменили знакомый маршрут автобуса, и теперь до школы надо идти пешком. Или поблизости открыли новую булочную, значит можно забегать в нее, а не идти в магазин в двух кварталах от дома. Или назначенную рабочую встречу перенесли на час, поэтому придется отменить поход в кино с друзьями, запланированный на вечер.
Все эти ситуации объединяет нечто общее — в окружающей среде возникли изменения, которые требуют от нас изменения поведения.Проблемы такого рода — когда меняющиеся обстоятельства заставляют менять способ их решения — возникали перед людьми задолго до того, как хлеб начали покупать в магазинах или даже печь его в печи. Изменения, происходящие в окружающей среде, постоянно подталкивают животных (и люди здесь не исключение) проявлять гибкость в достижении результата. В научной литературе приспособление поведения к меняющимся условиям получило название когнитивной, или поведенческой, гибкости (англ. cognitive (behavioral) flexibility). Если эта способность нарушена — из-за травмы головного мозга, в результате неблагоприятного воздействия (отравление, инфекционное заболевание, радиационное облучение и проч.) или при старении, — поведение становится менее гибким, животные как бы застревают в прошлом, продолжая использовать ставшие неэффективными способы достижения цели.
Эти проявления поведенческой ригидности вызваны изменениями, происходящими на разных уровнях организации нервной системы. Известно, что те же неблагоприятные воздействия, а также старение организма приводят к широкому спектру нарушений на клеточном и молекулярном уровне. Особой чувствительностью к ним отличается процесс появления новых нейронов из стволовых клеток мозга — нейрогенез. Во взрослом мозге нейрогенез идет в нескольких регионах: в субвентрикулярной и субгранулярной зонах зубчатой извилины гиппокампа, а также в обонятельной луковице. И хотя роль взрослорожденных нейронов (ВРН) в обучении и запоминании новой информации описана в научной литературе достаточно подробно (J. B. Aimone et al., 2011. Resolving new memories: a critical look at the dentate gyrus, adult neurogenesis, and pattern separation; J. B. Aimone et al., 2014. Regulation and function of adult neurogenesis: from genes to cognition; K. G. Akers et al., 2014. Hippocampal neurogenesis regulates forgetting during adulthood and infancy; J. R. Epp et al., 2016. Neurogenesis-mediated forgetting minimizes proactive interference; C. D. Clelland et al., 2009. A functional role for adult hippocampal neurogenesis in spatial pattern separation), по-прежнему мало известно о взаимосвязи между нарушением нейрогенеза и когнитивной гибкостью. Группа ученых из Университета штата Нью-Йорк в Стони-Бруке (США), НИИ нормальной физиологии им. П. К. Анохина, Института перспективных исследований мозга МГУ и Института высшей нервной деятельности и нейрофизиологии РАН исследовала этот вопрос.
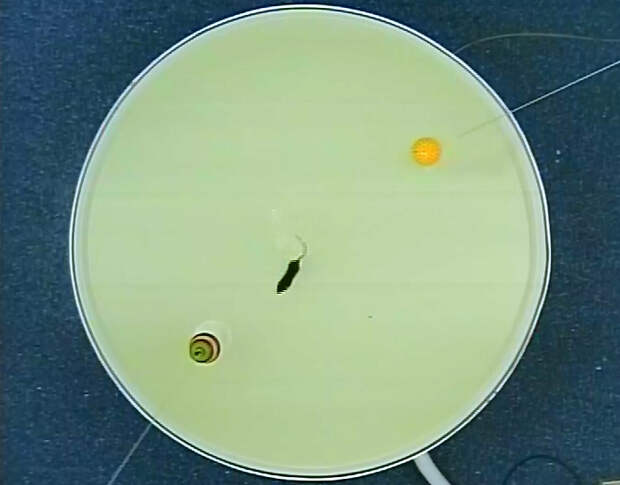
Одной из важных причин, по которым эта тема была мало исследована, являлось небольшое количество методик исследования когнитивной гибкости в поведении животных: существовавшие поведенческие модели оказывались нечувствительны к дефициту ВРН, то есть животные, несмотря на сниженный нейрогенез, могли успешно обучаться в них. Исходя из того, что гиппокамп млекопитающих — одна из структур мозга, в которой в течение жизни идет нейрогенез и которая критически необходима для навигации в пространстве, мы решили использовать водный лабиринт Морриса (Morris water maze, MWM) в качестве основы для разработки новой поведенческой модели. В классической версии, опубликованной британским нейробиологом Ричардом Моррисом (Richard G. Morris) в 1981 году, крыс помещают в бассейн диаметром два метра, наполненный водой. Хотя крысы — хорошие пловцы, они всё же стараются быстрее оказаться на суше. Для этого животные должны найти небольшую (10 см в диаметре) платформу, установленную в бассейне и не видимую с уровня воды, и выбраться на нее — поэтому модель называют «водным лабиринтом». Животных учат вплавь находить платформу, давая им несколько ежедневных попыток (продолжительность попытки не больше одной минуты). Обучение длится несколько дней, при этом видно, что поиск платформы занимает у грызунов всё меньше времени. Чтобы находить платформу, они запоминают расположение объектов, окружающих бассейн (так называемых «внешних ориентиров»; ими могут быть предметы мебели, плакаты на стенах, окна и проч.), и используют их для ориентации в пространстве — как мореходы использовали звёзды для навигации.
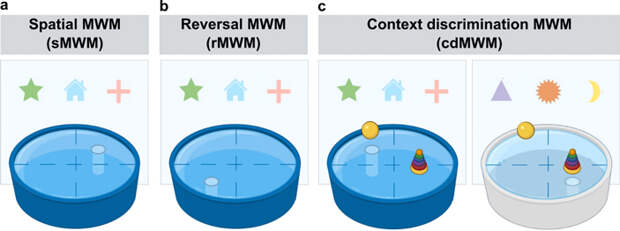
Используя водный лабиринт Морриса как основу, мы предложили следующую модель для оценки когнитивной гибкости. Животные (в наших экспериментах это были мыши) выучивали положение платформы в нескольких сессиях обучения (рис. 1): сначала в классической пространственной версии лабиринта Морриса, описанной выше (spatial MWM, sMWM, рис. 1а), затем мы меняли местоположение платформы (первое переучивание, reversal MWM, rMWM, рис. 1b), а когда мыши, адаптируясь к новым условиям, выучивали и его, задачу снова меняли, дополнительно усложняя ее. На этот раз мышей обучали попеременно в двух бассейнах: знакомом — том, в котором они учились искать платформу до этого, — и новом, расположенном в соседней комнате с незнакомыми пространственными ориентирами. Во время этого второго переучивания над каждым бассейном вывешивали по паре предметов (их называют «маячками», или локальными ориентирами; мы использовали две яркие игрушки, одинаковые для обоих бассейнов). Платформа в одном бассейне была расположена под одним маячком, в другом бассейне — под другим (рис. 1c). Таким образом, мы ожидали, что животные продемонстрируют способность отличить две обстановки (context discrimination MWM, cdMWM), используя сочетание внешних и локальных ориентиров для поиска платформы.
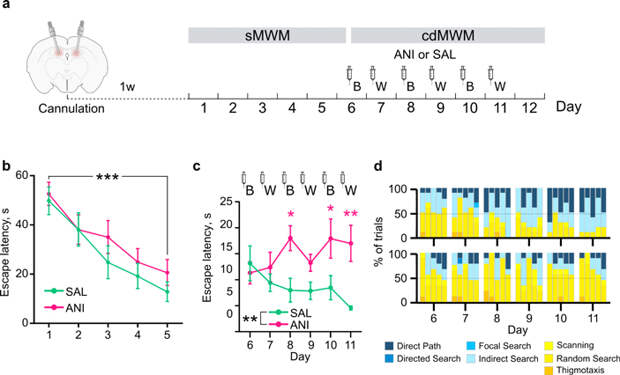
В предварительном эксперименте необходимо было выяснить, способны ли обученные животные научиться отличить две обстановки, если нарушить работу зубчатой извилины в целом. Это дало бы нам основания двигаться дальше, уточняя, как снижение нейрогенеза влияет на когнитивную гибкость. Мышей сначала обучили находить платформу в одном бассейне, затем им предстояло научиться находить платформу в ежедневно чередующихся синем (B) и белом (W) бассейнах (рис. 2a). При этом мыши одной группы получали инъекцию антибиотика анизомицина (Anisomycin, ANI) в зубчатую извилину гиппокампа перед началом каждой сессии переучивания (дни с 6-го по 11-й), мыши другой (контрольной) группы получали инъекцию физиологического раствора (SAL). Известно, что анизомицин не только нарушает электрическую активность нейронов, но и подавляет синтез белка, который является важным компонентом каскада молекулярных событий, ведущих к формированию долговременной памяти. Мы обнаружили, что животные группы ANI тратили больше времени, чем контрольные мыши, на поиск платформы в версии лабиринта Морриса с различением обстановок (рис. 2с).
По видеозаписям попыток поиска платформы мы анализировали траектории движения мышей в бассейнах (поведенческие стратегии), чтобы оценить, насколько эффективна была их навигация. Мы выделили два класса стратегий поиска платформы: эффективный (на рис. 2d показаны оттенками синего; мышь плывет прямо к платформе или незначительно отклоняется от прямой) и неэффективный (на рис. 2d показаны оттенками желтого; мышь делает много ошибок в поисках платформы или плавает вдоль стенки бассейна), см. примеры на видео. Эффективный класс стратегий включал в себя: прямой путь (direct path), направленный поиск (directed search), сфокусированный поиск (focal search), ненаправленный поиск (indirect search). Неэффективный класс стратегий включал в себя: сканирующее плавание (scanning), случайный поиск (random search), тигмотаксис (thigmotaxis — плавание вдоль стенки бассейна); подробнее о классификации стратегий см. в статье M. B. Cooke et al., 2019. Pathfinder: open source software for analyzing spatial navigation search strategies.
Мы обнаружили, что животные группы ANI полагались в основном на менее эффективные стратегии, совершая много ошибок в поисках платформы (рис. 2d, нижняя диаграмма). В то же время у животных группы SAL по мере обучения увеличивалась доля эффективных стратегий (рис. 2d, верхняя диаграмма). Таким образом, мы сделали вывод о необходимости зубчатой извилины для различения обстановок (то есть для когнитивной гибкости) у обученных животных в водном лабиринте Морриса.
Имея в руках модель обучения, в которой животные должны постоянно адаптироваться к меняющимся условиям среды (то есть демонстрировать когнитивную гибкость) и которая зависит от зубчатой извилины, мы могли исследовать, как воздействия, нарушающие нейрогенез, сказываются на когнитивной гибкости. В качестве таких воздействий нами были выбраны гамма-излучение и естественное старение. Исследования прошлых лет установили, что и радиационное облучение, и старение драматичным образом снижают количество делящихся стволовых клеток, а также число ВРН в зубчатой извилине гиппокампа (M. L. Monje et al., 2002. Irradiation induces neural precursor-cell dysfunction; J. M. Encinas et al., 2008. Quiescent adult neural stem cells are exceptionally sensitive to cosmic radiation; O. A. Mineyeva et al., 2018. Radiation induces distinct changes in defined subpopulations of neural stem and progenitor cells in the adult hippocampus). Но вопрос о связи такого снижения нейрогенеза с когнитивной гибкостью был исследован мало.
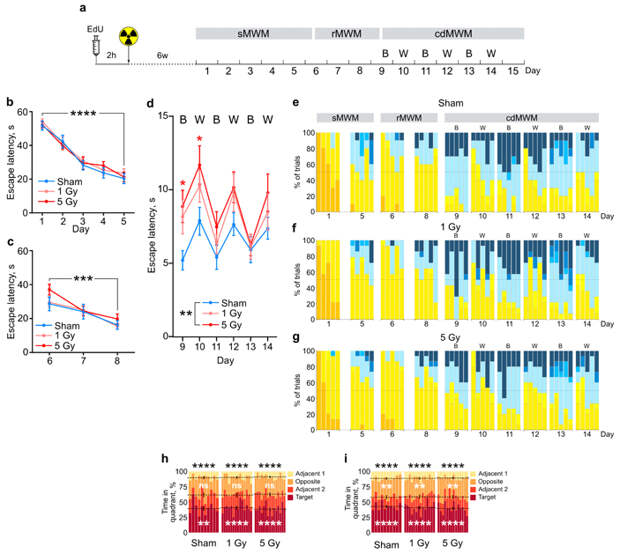
Из литературы известно, что ВРН через 4–8 недель после возникновения в мозге начинают активно встраиваться в существующие нейронные сети, устанавливая синаптические контакты с другими нейронами (см. обзор A. Denoth-Lippuner, S. Jessberger, 2021. Formation and integration of new neurons in the adult hippocampus). Поэтому мы решили исследовать, как отсутствие ВРН в возрасте четырех и шести недель может сказаться на когнитивной гибкости. Группы мышей были подвергнуты гамма-облучению в дозах 1 или 5 Гр, контрольная группа не была облучена, затем животные были обучены в разработанной поведенческой модели через четыре или шесть недель после облучения (рис. 3; приведены только данные эксперимента, начатого через шесть недель после облучения. Подробное описание см. в обсуждаемой статье в The Journal of Neuroscience).
Мы обнаружили, что обучение и первое переучивание в лабиринте Морриса не были нарушены через шесть недель (и через четыре недели) после облучения (рис. 3b, c). Однако мыши, облученные более высокой дозой 5 Гр, достоверно дольше, чем контрольные животные, искали платформу в версии с различением обстановок (рис. 3d). Кроме того, они больше использовали неэффективные стратегии поиска платформы (рис. 3g, по сравнению с рис. 3e, на котором показаны стратегии поиска контрольной группы). Это нарушение было временным и ярче всего проявилось 9-й и 10-й день эксперимента, когда мыши впервые оказались в новой ситуации, требующей отличить одну обстановку от другой. По мере переучивания животные облученной группы догоняли необлученных.
После окончания обучения мы протестировали память мышей, помещая их на одну минуту в бассейн без платформы. (Эта попытка выполняется в конце обучения, чтобы выяснить, в каком месте бассейна животные проводят больше времени; если они плавают в том месте, где платформа была во время обучения, можно сделать вывод, что их память не нарушена.) Группы практически не отличались друг от друга, плавая в основном в квадранте бассейна, где они находили платформу при обучении (рис. 3h, i), то есть их память не была нарушена. Важно упомянуть, что облучение не повлияло на показатели физической активности животных: мы не обнаружили отличий в скорости плавания между группами облученных и необлученных мышей.
Как было сказано выше, ВРН необходимо не меньше четырех недель для созревания и интеграции в существующие нейронные сети мозга (см. обзор A. Denoth-Lippuner, S. Jessberger, 2021. Formation and integration of new neurons in the adult hippocampus). Поэтому было важно убедиться, что нарушение когнитивной гибкости, которое мы обнаружили в экспериментах через четыре и шесть недель, не происходит на более ранних сроках после облучения. Другими словами, наша гипотеза заключалась в следующем: нехватка нейронов, убитых облучением, не должна сказаться на когнитивной гибкости, если эти нейроны еще не успели стать активными участниками нейронных сетей мозга. В дополнительном эксперименте мы начинали обучение животных через одну неделю после облучения. Как мы и ожидали, животные облученной и необлученной (контрольной) групп не отличались друг от друга на всех этапах обучения и переучивания. Это свидетельствовало о том, что, хотя радиация и убила делящиеся клетки и, вероятно, некоторые незрелые нейроны, но поскольку обучение происходило раньше, чем они встроились в существующие сети мозга, нехватка этих клеток не повлияла на выполнения задачи, требующей когнитивной гибкости.
Чтобы убедиться в подавлении нейрогенеза облучением, необходимо сравнить нейрогенез у облученных и контрольных животных. Для этого перед началом эксперимента мы вводили мышам тимидиновую метку — аналог тимидина этинилдезоксиуридин (EdU, рис. 2а). Аналоги тимидина — это группа соединений, которые встраиваются в цепь ДНК при ее репликации, предшествующей делению клетки. Дочерние клетки можно выявить по включению тимидиновой метки, используя методы гистохимического окрашивания. Помимо делящихся клеток, нас интересовало, сколько ВРН появилось после облучения. На разных этапах созревания нейроны экспрессируют разные белки, которые, как и тимидиновые аналоги, можно выявить благодаря гистохимическому окрашиванию ткани. Для незрелых нейронов характерна экспрессия белка даблкортина (Doublecortin, DCX), тогда как зрелые нейроны экспрессируют белок NeuN (при этом только те нейроны, в которых одновременно будут обнаружены EdU и NeuN, являются зрелыми ВРН). Подсчет количества выживших делившихся клеток, незрелых и зрелых ВРН в мозге мышей показал, что этих типов клеток было достоверно меньше у мышей, облученных дозами 1 Гр и 5 Гр, по сравнению с необлученными контрольными мышами, что подтвердило эффективность выбранной дозы гамма-излучения в подавлении нейрогенеза в мозге взрослых мышей.
Таким образом, в описанных сериях экспериментов мы выяснили, что гамма-облучение приводило к подавлению нейрогенеза и к ухудшению когнитивной гибкости (но не обучения) в пространственной задаче. Это нарушение проявлялось через четыре и шесть, но не через одну неделю после облучения и носило временный характер. Дополнительное обучение позволяло компенсировать нарушение: показатели поведения облученных животных догоняли показатели контрольных, необлученных мышей.
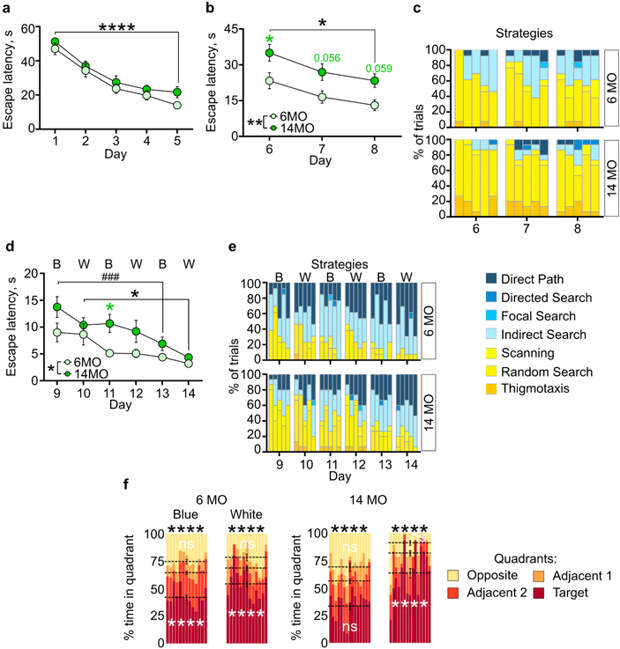
К снижению нейрогенеза могут приводить не только внешние воздействия (такие, как радиация). Наши ранние данные и данные других групп свидетельствуют о том, что с возрастом происходит резкое и необратимое подавление числа делящихся стволовых клеток и ВРН в мозге (H. G. Kuhn et al., 1996. Neurogenesis in the dentate gyrus of the adult rat: age-related decrease of neuronal progenitor proliferation; J. M. Encinas et al. 2011. Division-coupled astrocytic differentiation and age-related depletion of neural stem cells in the adult hippocampus; M. Boldrini et al., 2018. Human hippocampal neurogenesis persists throughout aging). Поэтому во второй работе, опубликованной в журнале Frontiers in Neuroscience, мы исследовали возможную связь между когнитивной гибкостью и уровнем нейрогенеза у пожилых животных. Мы использовали мышей двух возрастов: 6 и 14 месяцев. В условиях вивария срок жизни мыши может достигать 24 месяцев, а признаки старения в виде ожирения, нарушения координации, хронических воспалительных процессов в мозге и нарушения памяти начинают проявляться с 18 месяцев. Таким образом, у животных выбранных нами возрастов мы не ожидали увидеть когнитивных нарушений. И действительно, мыши обеих групп успешно обучились в стандартной версии лабиринта Морриса (рис. 4a).
Однако уже во время первого переучивания, при перестановке платформы на новое место в знакомом бассейне, пожилые мыши продемонстрировали отставание от более молодых животных (рис. 4b). Они чаще использовали неэффективные стратегии поиска платформы (рис. 4с). Эти нарушения проявились и во время второго переучивания, когда от мышей требовалось отличить две обстановки. 14-месячные животные дольше (рис. 4d) и менее эффективно (рис. 4e) искали платформу, чем 6-месячные животные. Мы контролировали физическое состояние животных в течение всего эксперимента и не обнаружили отличий в скорости плавания между группами молодых и пожилых мышей. Интересно, что, как и в экспериментах с облученными мышами, дефицит обучения был временным, преодолевался при продолжении обучения и не приводил к нарушению памяти (рис. 4f).
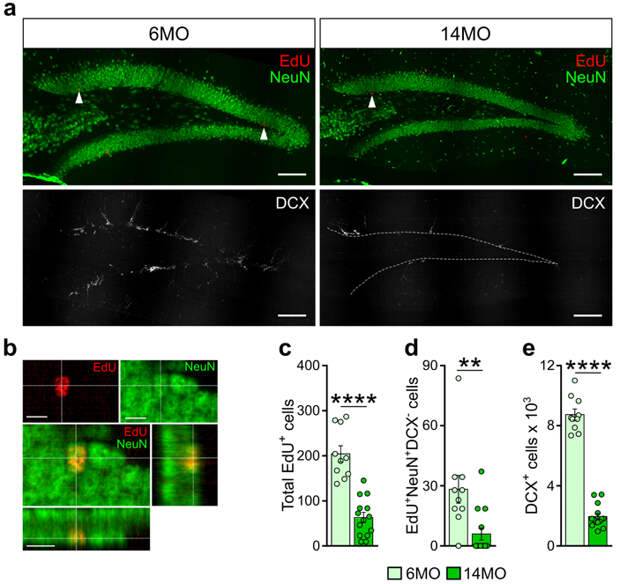
Чтобы проверить гипотезу о связи между когнитивной гибкостью и возрастным падением нейрогенеза, необходимо было проанализировать количество выживших делившихся клеток и ВРН у животных 6 и 14 месяцев (рис. 5). Для этого, как и в эксперименте с облучением, мышам вводили EdU за 6 недель до начала обучения, чтобы пометить делящиеся клетки. Также анализировали количество клеток, экспрессирующих DCX и NeuN (рис. 5a, b). После окончания обучения мы подсчитывали количество выживших делившихся клеток (рис. 5с), зрелых (рис. 5d) и незрелых ВРН (рис. 5e). Выяснилось, что у 14-месячных животных клеток всех типов было достоверно меньше, чем у 6-месячных животных, что говорило о существенном подавлении нейрогенеза с возрастом.
Наконец, корреляционный анализ количества клеток разных типов и показателей обучения в трех последовательных версиях лабиринта Морриса позволил установить наличие корреляций между количеством незрелых и зрелых ВРН с временем достижения платформы и с количеством использованных эффективных стратегий поиска платформы, но только в ситуациях, требовавших проявления когнитивной гибкости (то есть при переучиваниях), а не при первоначальном обучении в лабиринте Морриса. Это свидетельствует о существовании связи между уровнем нейрогенеза и способностью животных демонстрировать когнитивную гибкость.
Таким образом, в серии работ нам удалось исследовать связь между уровнем нейрогенеза во взрослом мозге и способностью мышей адаптироваться к меняющимся условиям среды. Существенное падение нейрогенеза в результате облучения или при естественном старении сопровождалось снижением показателей когнитивной гибкости. Животные со сниженным нейрогенезом, тем не менее, были способны наверстать показатели контрольных групп при продолжении обучения, что может свидетельствовать об ограниченной роли взрослорожденных нейронов в модификации прошлого опыта. Наконец, нами была установлена связь между уровнем нейрогенеза (по количеству ВРН разной степени зрелости) и поведением животных в ситуации, требующей проявления когнитивной гибкости. В будущем мы собираемся исследовать связь нейрогенеза и когнитивной гибкости в более естественных для мышей условиях, не требующих плавания, а также установить, как ВРН разных возрастов устанавливают связи в сетях мозга и влияет ли это на их участие в адаптивном поведении.
Источники:
1) Evgeny M. Amelchenko, Dmitri V. Bezriadnov, Olga A. Chekhov, Anna A. Ivanova, Alexander V. Kedrov, Konstantin V. Anokhin, Alexander A. Lazutkin and Grigori Enikolopov. Cognitive Flexibility Is Selectively Impaired by Radiation and Is Associated with Differential Recruitment of Adult-Born Neurons // The Journal of Neuroscience. August 23, 2023. V. 43(34). P. 6061–6083. DOI: 10.1523/JNEUROSCI.0161-22.2023.
2) Evgeny M. Amelchenko, Dmitri V. Bezriadnov, Olga A. Chekhov, Konstantin V. Anokhin, Alexander A. Lazutkin and Grigori Enikolopov. Age-related decline in cognitive flexibility is associated with the levels of hippocampal neurogenesis // Frontiers in Neuroscience. 14 August 2023. V. 17. 1232670. DOI: 10.3389/fnins.2023.1232670.
Евгений Амельченко





Свежие комментарии