Российские ученые создали модель биохимического процесса, который происходит в клетках мозга на начальных этапах развития старческой деменции. Эксперимент подтвердил теорию о том, что причина возрастных расстройств — действие свободных радикалов в нервных клетках. Разработки позволят на ранних стадиях диагностировать такие патологии как болезни Альцгеймера и Паркинсона. Уже сейчас на предложенной модели можно тестировать препараты от возрастных заболеваний мозга. Результаты исследований, поддержанных грантами Российского научного фонда (РНФ) опубликованы в журнале Redox Biology.
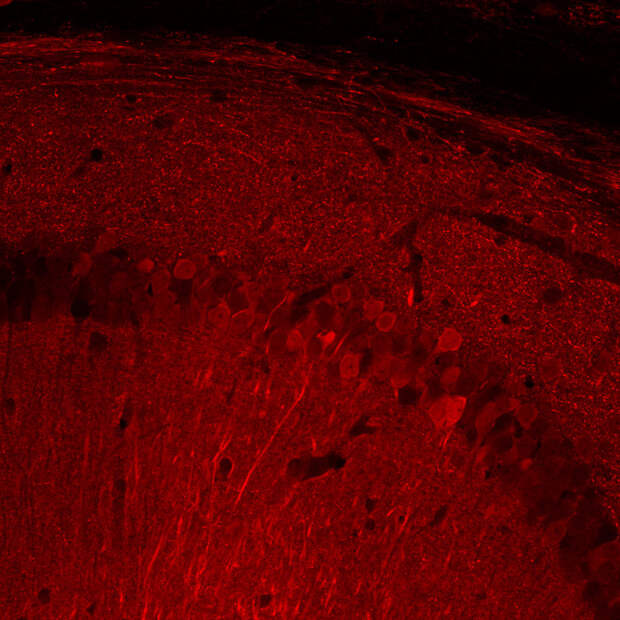
От старческой деменции страдают около 50 миллионов человек во всем мире. В 1% случаев врачи отмечаютнаследственную предрасположенность к заболеванию. Но пока неизвестно, что именно запускает процесс разрушения нервных клеток в подавляющем большинстве случаев и почему одни люди подвержены ему больше других. Кроме того, возрастные психические нарушения обычно диагностируются после 65 лет, и распознать развитие деменции в более раннем возрасте сложно. При этом ученые давно обнаружили, что первые признаки заболевания, такие как снижение памяти и способности к обучению, сопровождаются окислительным стрессом в клетках мозга. Он возникает, когда в стареющем организме снижается количество антиоксидантных ферментов и образуется избыток свободных радикалов — активных форм кислорода, которые вступают в реакции с молекулами живой клетки, разрушая ее.
До сих пор оставалось неясным, является это причиной заболеваний, их симптомом или сопутствующей патологией. Изучение вопроса затрудняла невозможность напрямую наблюдать и контролировать химические процессы, происходящие в живом мозге.Группа ученых на базе Института биоорганической химии имени М.М. Шемякина и Ю.А. Овчинникова Российской академии наук (Москва) воссоздала контролируемый окислительный стресс в отдельных клетках мозга мышей. Для этого был создан искусственный вирус, который выступает носителем особой генетической конструкции. Она обеспечивает нейроны программой, записанной в ДНК, благодаря которой в вирусах вырабатывается фермент оксидаза D-аминокислот. На искусственно выращенных нейронах, зараженных вирусом, ученые проверили, что добавление к ним вещества D-норвалина вызывает выделение пероксида водорода — самой долгоживущей в клетке молекулы, относящейся к активным формам кислорода. После вирус с помощью микрошприца ввели в гиппокамп лабораторных мышей, чтобы выяснить, какие изменения вызывает окислительный стресс в живом мозге.
Через две недели у зараженных вирусом животных взяли срезы мозга толщиной 300 мкм. Анализ образцов включал микроскопическое исследование и электрофизиологические эксперименты: ученые вызывали окислительный стресс в конкретном нейроне и регистрировали электрическую активность этого нейрона. Во всех случаях наблюдалось снижение синаптической пластичности — способности нервных клеток усиливать или ослаблять связь между нейронами и регулировать скорость передачи нервных импульсов. Это свойство клеток ученые связывают со способностью млекопитающих к обучению и запоминанию.
Модель развития деменции на уровне клеток построена учеными впервые и позволяет определить признаки заболевания на ранних этапах. В будущем это поможет диагностировать психическую дегенерацию в самом начале, когда у пациента еще не проявились когнитивные нарушения.
«То, что мы сделали на срезах мозга — это готовая платформа для проверки лекарственных препаратов, которые бы улучшали функции нервных клеток в условиях окислительного стресса. Следующим шагом будет получение доказательств, что этот процесс в клетках мозга приводит к развитию болезни Альцгеймера. Для этого мы будем наблюдать за животными, чтобы понять, как изменяются их когнитивные функции после воздействия нашего инструмента», — рассказывает Олег Подгорный, кандидат биологических наук, старший научный сотрудник ИБХ РАН. В исследовании также приняли участие ученые из Московского государственного университета имени М.В. Ломоносова (Москва), Института фундаментальной неврологии Федерального центра мозга и нейротехнологий Федерального медико-биологического агентства (Москва), Казанского федерального университета (Казань), Российского национального исследовательского медицинского университета имени Н.И. Пирогова (Москва), Института биологии и биомедицины Нижегородского государственного университета имени Н.И. Лобачевского(Нижний Новгород), Центра высокоточного редактирования и генетических технологий для биомедицины РНИМУ им. Н.И. Пирогова (Москва), Института высшей нервной деятельности и нейрофизиологии Российской академии наук (Москва) совместно с коллегами из Гейдельбергского университета и Геттингенского университета имени Георга Августа (Германия).
Текст: пресс-служба РНФ
Kalinichenko, A. L., Jappy, D., Solius, G. M., Maltsev, D. I., Bogdanova, Y. A., Mukhametshina, L. F., Sokolov, R. A., Moshchenko, A. A., Shaydurov, V. A., Rozov, A. v., Podgorny, O. v., & Belousov, V. v. (2023). Chemogenetic emulation of intraneuronal oxidative stress affects synaptic plasticity. Redox Biology, 60, 102604. https://doi.org/10.1016/j.redox.2023.102604
Свежие комментарии